题目内容
在碳酸钠溶液中通二氧化碳,会发生如下反应:Na2CO3+CO2+H2O=2NaHCO3.若已知20℃时Na2CO3的溶解度是21.5g,NaHCO3的溶解度是9.6g,则在20℃的碳酸钠饱和溶液中通二氧化碳一段时间后会看到什么现象?简述理由.
答案:
解析:
解析:
|
溶液会变浑,根据化学方程式中各物质质量比,每反应106g Na2CO3,能生成168g NaHCO3,而NaHCO3溶解度小于Na2CO3,因此变浑是生成的NaHCO3不能完全溶解所致. |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
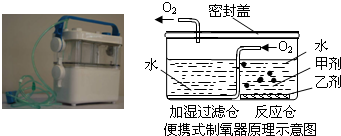 小雨对爸爸给患病的奶奶购买的“便携式制氧器”(如图)产生浓厚的兴趣,他仔细阅读说明书,了解了它的工作原理(如图)和所用的药品.药品中甲剂是一种白色颗粒状固体,作制氧剂;乙剂是黑色固体,作催化剂.
小雨对爸爸给患病的奶奶购买的“便携式制氧器”(如图)产生浓厚的兴趣,他仔细阅读说明书,了解了它的工作原理(如图)和所用的药品.药品中甲剂是一种白色颗粒状固体,作制氧剂;乙剂是黑色固体,作催化剂.【提出问题】甲剂的化学成分是什么?
【查阅资料】过碳酸钠是白色颗粒状固体,溶于水时,生成碳酸钠和过氧化氢,可用于制取氧气.
【设计与实验】小雨把甲剂和乙剂带到实验室与黄老师共同探究.在老师的指导下,验证出甲剂是一种钠盐后,小雨接着进行如下实验:
(实验一]用甲剂和乙剂制取并验证氧气.
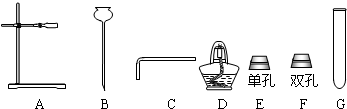
(1)根据图得出:
①组装气体发生装置时应选择图中所示的仪器:
②氧气具有的性质是
(2)装置连接完毕,装药品前应先检查装置的
(3)小雨认为氧气是由过氧化氢在乙剂催化下产生的,其化学方程式为:
(4)如何验证收集到的气体是氧气?(简述实验操作与现象)
(实验二]检验上述反应后的溶液中含有碳酸根离子.
| 检验步骤 | 实验操作 | 实验现象 | 结论 |
| 步骤一 | 取少量反应后的溶液,加入稀盐酸 | 有气泡产生 | |
| 步骤二 | 将步骤一产生的气体通入澄清石灰水 | 澄清石灰水变浑浊 |
【反思与评价】小方认为小雨的结论不够严密,你认为严密的结论应该是