题目内容
17.利用化学反应2Na+H2$\frac{\underline{\;\;△\;\;}}{\;}$2NaH可实现氢气的存储:(1)计算230g金属钠最多可吸收氢气的质量;
(2)NaH中氢元素的化合价是-1;
(3)NaH中阳离子的结构示意图为
 .
.
分析 (1)根据反应的化学方程式和钠的质量,可以计算吸收氢气的质量;
(2)根据化合物中正负化合价的代数和为零解答;
(3)根据原子结构示意图的表示法:小圆圈和圈内的数字表示原子核和核内质子数;弧线表示电子层,弧线上的数字该电子层上的电子数,进行解答.
解答 解:设可吸收氢气的质量为x,
2Na+H2$\frac{\underline{\;\;△\;\;}}{\;}$2NaH
46 2
230g x
$\frac{46}{230g}=\frac{2}{x}$
x=10g.
(2)NaH中钠元素的化合价显+1价,故氢元素的化合价显-1价;
(3)钠离子核内有11个质子,核外有两个电子层,第一层两个电子,第二层八个电子,故其图示为:
答案:
(1)可吸收氢气的质量为10g;
(2)-1;
(3)
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
5.下列气体,不属于温室气体的是( )
| A. | CO2 | B. | O3 | C. | N2 | D. | CH4 |
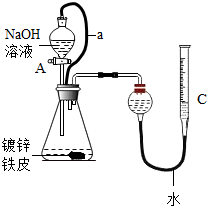 “白铁皮”是一种广泛应用于生产生活的金属材料. 某班级分两个兴趣小组开展了对“白铁皮”相关性质及应用的调查研究活动.
“白铁皮”是一种广泛应用于生产生活的金属材料. 某班级分两个兴趣小组开展了对“白铁皮”相关性质及应用的调查研究活动.
 有A、B、C三种物质,已知A是一种氯化物,B为一种钠盐,C是一种可溶性碱.如图所示是A、B、C的溶液两两反应的实验现象.
有A、B、C三种物质,已知A是一种氯化物,B为一种钠盐,C是一种可溶性碱.如图所示是A、B、C的溶液两两反应的实验现象. 如图是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态,化合物D的水溶液呈浅绿色.
如图是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态,化合物D的水溶液呈浅绿色.