题目内容
16.向盛有26.4g的硫酸钠和碳酸钠混合物的烧杯中加入218g稀硫酸,恰好完全反应,固体全部消失,烧杯内物质总质量减少了4.4g.该化学反应方程式如下:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑(要求写出计算过程).(1)原混合物中碳酸钠的质量.
(2)反应后所得溶液中溶质的质量分数.
分析 烧杯内物质总质量减少了4.4g,说明碳酸钠和稀硫酸反应生成了4.4g二氧化碳,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)设碳酸钠质量为x,反应生成硫酸钠质量为y,
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑,
106 142 44
x y 4.4g
$\frac{106}{x}$=$\frac{142}{y}$=$\frac{44}{4.4g}$,
x=10.6g,y=14.2g,
答:原混合物中碳酸钠的质量是10.6g.
(2)反应后所得溶液中溶质的质量分数为:$\frac{26.4g-10.6g+14.2g}{26.4g+218g-4.4g}$×100%=12.5%,
答:反应后所得溶液中溶质的质量分数为12.5%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
6.属于可溶性碱的是( )
| A. | Mg(OH)2 | B. | KOH | C. | Cu(OH)2 | D. | Al(OH)3 |
7.四氧化三铁可用于医疗器械、电子等工业.某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验.
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表.
(2)25℃时,Zn(OH)2可溶于pH>10.5的碱溶液.
(3)制备Fe3O4的实验流程如图:

【回答问题】
(1)操作a的名称为过滤.该操作需要的玻璃仪器有烧杯、玻璃棒、漏斗等.玻璃棒在此操作中的主要作用是引流.
(2)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4,或2NaOH+FeSO4=Fe(OH)2↓+Na2SO4(写一个即可).
(3)溶液1所含溶质有硫酸镁、硫酸钠和氢氧化钠.
(4)该实验取废液100g,最终得到产品四氧化三铁质量为4.64g,则原废液中硫酸亚铁溶质的质量分数不低于9.12%(精确到0.01%).
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表.
| Zn(OH)2 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀的pH | 5.7 | 7.6 | 10.4 |
| 沉淀完全的pH | 8.0 | 9.6 | 12.4 |
(3)制备Fe3O4的实验流程如图:

【回答问题】
(1)操作a的名称为过滤.该操作需要的玻璃仪器有烧杯、玻璃棒、漏斗等.玻璃棒在此操作中的主要作用是引流.
(2)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4,或2NaOH+FeSO4=Fe(OH)2↓+Na2SO4(写一个即可).
(3)溶液1所含溶质有硫酸镁、硫酸钠和氢氧化钠.
(4)该实验取废液100g,最终得到产品四氧化三铁质量为4.64g,则原废液中硫酸亚铁溶质的质量分数不低于9.12%(精确到0.01%).
4.下列微粒结构示意图中,表示阴离子的是( )
| A. |  | B. |  | C. |  | D. |  |
11.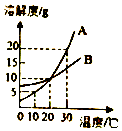 如图是A、B两种物质的溶解度曲线,下列叙述正确的是( )
如图是A、B两种物质的溶解度曲线,下列叙述正确的是( )
 如图是A、B两种物质的溶解度曲线,下列叙述正确的是( )
如图是A、B两种物质的溶解度曲线,下列叙述正确的是( )| A. | A物质的溶解度大于B物质的溶解度 | |
| B. | A物质的饱和溶液从30℃降温到20℃,其溶质质量分数不变 | |
| C. | 30℃时,向100克水中加入25克A物质,充分溶解后所得的溶液质量为125克 | |
| D. | 30℃时,将B物质的不饱和溶液转变为饱和溶液,可用恒温蒸发溶剂的方法 |
1.下列有关资源及能源的说法正确的是( )
| A. | 目前人类制得的纯金属有90余种,人类每年在自然界中提取最多的金属是铁 | |
| B. | 空气是一种重要的自然资源,它是由氧气和氮气两种气体组成的 | |
| C. | “西气东输”输送的是液化石油气 | |
| D. | 只有节约用水才能防止水污染 |
6.下列有关置换反应现象的描述正确的是( )
| A. | 将铁丝插入硫酸铜溶液中观察到铁丝表面有银白色物质生成 | |
| B. | 把用砂纸打磨过的铝片放入稀硫酸中,观察到有气泡产生,溶液由无色变为浅绿色 | |
| C. | 把铜丝插入硝酸银溶液中,铜丝表面有银白色固体生成,溶液由无色变为蓝色 | |
| D. | 将铜片放入稀盐酸中,有大量的气泡产生 |