题目内容
4. 为探究水的组成,化学实验小组进行如下实验.
为探究水的组成,化学实验小组进行如下实验.【实验装置】如图所示.
【进行实验】按如图连接好实验装置,闭合电源,观察到a、b两管均产生气体,且b(填“a”或“b”)管产生气泡速率较快.用燃着的木条检验b管收集的气体,观察到的现象是气体能燃烧,产生淡蓝色的火焰.
【得出结论】水由氢元素和氧元素组成,写出反应的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
【讨论与交流】
(1)电解水时,最好先在水中加入硫酸钠.目的是增强水的导电性.
(2)已知同温同压下,气体的体积比决定于气体的分子个数比,该实验中能说明水的化学式为“H2O”的实验现象是生成的氢气和氧气的体积比是2:1.
分析 根据电解水试验的现象和结论以及注意事项分析回答有关问题,电解水时“正氧负氢,氢二氧一”
解答 解:【进行实验】电解水时“正氧负氢,氢二氧一”;按如图连接好实验装置,闭合电源,观察到a、b两管均产生气体,b产生的气体多是氢气具有可燃性,所以b管产生气泡速率较快.用燃着的木条检验b管收集的气体,观察到的现象是:气体能燃烧,产生淡蓝色的火焰.
【得出结论】电解水生成了氢气和氧气,说明了水是由氢元素和氧元素组成的,电解水反应的化学方程式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
【讨论与交流】
(1)电解水时,最好先在水中加入硫酸钠.目的是增强水的导电性.
(2)已知同温同压下,气体的体积比决定于气体的分子个数比,该实验中能说明水的化学式为“H2O”的实验现象是生成的氢气和氧气的体积比是2:1.
故答为:【进行实验】b,气体能燃烧,产生淡蓝色的火焰.
【得出结论】氢元素和氧元素,2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
【讨论与交流】
(1)增强水的导电性.(2)生成的氢气和氧气的体积比是2:1.
点评 本题的难度不大,了解电解水试验的现象、结论即生成气体的性质是解答本题的基础.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
12.下列与质量守恒定律有关的说法正确的是( )
| A. | 铝丝在氧气中燃烧后质量增加,不符合质量守恒定律 | |
| B. | 100g冰融化后质量仍为100g,符合质量守恒定律 | |
| C. | 某物质在空气中燃烧生成了 H2O和CO2,则该物质中一定含有C、H、O三种元素 | |
| D. | 化学反应前后原子的种类、数目和质量都不变,因此化学反应都遵守质量守恒定律 |
16.下列生活里的常见物品中,属于溶液的是( )
| A. | 果粒橙 | B. | 医用酒精 | C. | 乳胶漆 | D. | 芝麻酱 |
 为了验证二氧化碳的性质,某同学将实验中制取的二氧化碳气体导入A、B装置(如图),回答下列问题:
为了验证二氧化碳的性质,某同学将实验中制取的二氧化碳气体导入A、B装置(如图),回答下列问题: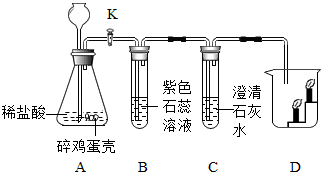 某校九年级(3)班的几个同学利用鸡蛋壳制取二氧化碳并对二氧化碳的性质进行验证,实验装置如图所示(鸡蛋壳的主要成分是碳酸钙).当打开K,反应一段时间后:
某校九年级(3)班的几个同学利用鸡蛋壳制取二氧化碳并对二氧化碳的性质进行验证,实验装置如图所示(鸡蛋壳的主要成分是碳酸钙).当打开K,反应一段时间后: 如图是某反应的微观模拟图,回答下列问题.
如图是某反应的微观模拟图,回答下列问题. 化学与我们日常生活密切相关,请结合实际填空,
化学与我们日常生活密切相关,请结合实际填空,