题目内容
15.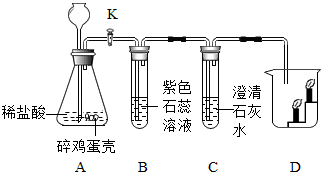 某校九年级(3)班的几个同学利用鸡蛋壳制取二氧化碳并对二氧化碳的性质进行验证,实验装置如图所示(鸡蛋壳的主要成分是碳酸钙).当打开K,反应一段时间后:
某校九年级(3)班的几个同学利用鸡蛋壳制取二氧化碳并对二氧化碳的性质进行验证,实验装置如图所示(鸡蛋壳的主要成分是碳酸钙).当打开K,反应一段时间后:(1)B处可以观察到的现象是溶液变为红色;
(2)C处澄清石灰水变浑浊,写出反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O;
(3)D处烧杯中下层(填“上层”或“下层”)的蜡烛先熄灭,说明二氧化碳具有的性质是二氧化碳的密度大于空气的密度;二氧化碳不燃烧也不支持燃烧.
分析 (1)根据显酸性的溶液能使石蕊试液变红色进分析;
(2)根据二氧化碳能使澄清石灰水变浑浊进行分析;
(3)根据实验现象可以判断二氧化碳的物理性质和化学性质;
解答 解:(1)二氧化碳能和水反应生成碳酸,碳酸能使紫色石蕊溶液变红,故B处紫色石蕊溶液变成红色;
(2)二氧化碳能和氢氧化钙溶液反应生成碳酸钙沉淀和水,该反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)二氧化碳不燃烧也不支持燃烧以及二氧化碳的密度大于空气的密度,所以D烧杯中下层的蜡烛先熄灭.故填:下层;二氧化碳的密度大于空气的密度;二氧化碳既不燃烧,也不支持燃烧.
故答案为:
(1)溶液变为红色;
(2)Ca(OH)2+CO2═CaCO3↓+H2O;
(3)下层;二氧化碳的密度大于空气的密度;二氧化碳不燃烧也不支持燃烧;
点评 本题是课本知识内容的再现,主要训练有关二氧化碳性质的熟练掌握程度,考查内容简单注重基础.

练习册系列答案
相关题目
10.下列各组物质中,前者属于混合物,后者属于纯净物的是( )
| A. | 洁净的空气 蒸馏水 | B. | 钢铁 汽油 | ||
| C. | 水银 液氮 | D. | 甲烷 醋酸 |
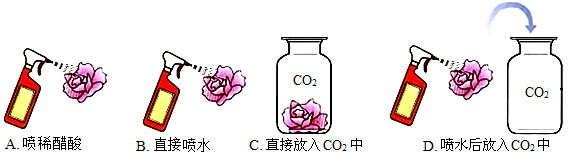

 为探究水的组成,化学实验小组进行如下实验.
为探究水的组成,化学实验小组进行如下实验. 如图是实验室制取气体的常用装置.
如图是实验室制取气体的常用装置.