题目内容
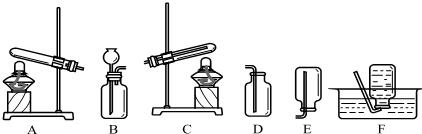
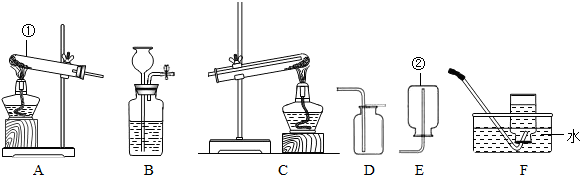
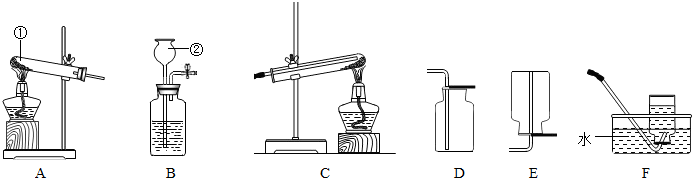
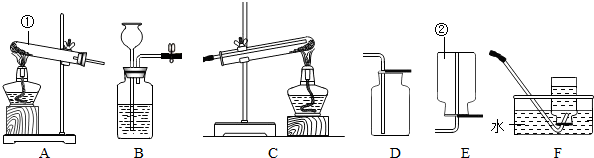
现有如图所示的下列实验装置.回答问题:
(1)仪器①的名称是______;仪器②的一种用途是______.
(2)若用氯酸钾和二氧化锰的混合物来制氧气,反应方程式为______△2KCl+3O2↑
【答案】分析:(1)根据常用仪器的名称和用途进行分析;
(2)根据氯酸钾分解的反应原理书写方程式,氯酸钾受热生成氧气,属于“固体加热型”,再依据氧气的密度和溶解性选择收集装置;
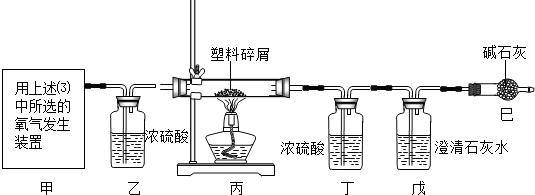
(3)根据催化剂的特点“一变两不变”(即在反应中能改变化学反应速率,而本身的质量和化学性质不变)分析解答;步骤①的目的是与③对比,研究铁锈是否改变化学反应速率;过滤用到的仪器有铁架台、烧杯、漏斗、玻璃棒;根据铁锈的主要成分是氧化铁,结合题意及氧化铁的化学性质设计实验.
解答:解:(1)根据常用仪器的名称和用途可知:仪器①是试管,②是集气瓶,集气瓶的主要作用是收集或贮存气体;
故答案为:试管; 收集或贮存气体;
(2)氯酸钾在二氧化锰作催化剂、加热的条件下生成氯化钾和氧气,方程式是2KClO3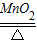 2KCl+3O2↑;氯酸钾受热生成氧气,属于“固体加热型”,故选发生装置A,氧气的密度比空气大且不易溶于水,所以可用向上排空气法和排水法收集;
2KCl+3O2↑;氯酸钾受热生成氧气,属于“固体加热型”,故选发生装置A,氧气的密度比空气大且不易溶于水,所以可用向上排空气法和排水法收集;
故答案为:2KClO3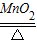 2KCl+3O2↑; A; D 或F;
2KCl+3O2↑; A; D 或F;
(3)根据题意:铁锈是该反应的催化剂,根据催化剂的特点“一变两不变”,所以其质量和化学性质在反应前后不变,其质量仍为0.2g,步骤①的目的是与③对比,研究铁锈是否改变化学反应速率;过滤用到的仪器有铁架台、烧杯、漏斗、玻璃棒;氧化铁可与还原性物质发生反应,还可与稀盐酸或稀硫酸反应,相比之下,与酸的反应简单易行,而与还原性物质要在加热或高温条件下进行,所以可取适量固体放于试管,然后倒入稀盐酸,若固体溶解,溶液变为黄色,说明氧化铁与稀盐酸可反应;
故答案为:
质量和化学性质不变;
铁锈的质量仍为0.2 g;
与步骤③对比; 玻璃棒; 取适量固体放于试管,然后倒入稀盐酸,若固体溶解,溶液变为黄色,说明氧化铁与稀盐酸可反应.
点评:本题综合性较强,既考查了装置的选取,方程式的书写,还考查了对于催化剂概念的理解,氧化铁的化学性质等知识,能很好的考查学生对知识的理解和应用.
(2)根据氯酸钾分解的反应原理书写方程式,氯酸钾受热生成氧气,属于“固体加热型”,再依据氧气的密度和溶解性选择收集装置;
(3)根据催化剂的特点“一变两不变”(即在反应中能改变化学反应速率,而本身的质量和化学性质不变)分析解答;步骤①的目的是与③对比,研究铁锈是否改变化学反应速率;过滤用到的仪器有铁架台、烧杯、漏斗、玻璃棒;根据铁锈的主要成分是氧化铁,结合题意及氧化铁的化学性质设计实验.
解答:解:(1)根据常用仪器的名称和用途可知:仪器①是试管,②是集气瓶,集气瓶的主要作用是收集或贮存气体;
故答案为:试管; 收集或贮存气体;
(2)氯酸钾在二氧化锰作催化剂、加热的条件下生成氯化钾和氧气,方程式是2KClO3
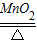 2KCl+3O2↑;氯酸钾受热生成氧气,属于“固体加热型”,故选发生装置A,氧气的密度比空气大且不易溶于水,所以可用向上排空气法和排水法收集;
2KCl+3O2↑;氯酸钾受热生成氧气,属于“固体加热型”,故选发生装置A,氧气的密度比空气大且不易溶于水,所以可用向上排空气法和排水法收集;故答案为:2KClO3
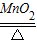 2KCl+3O2↑; A; D 或F;
2KCl+3O2↑; A; D 或F;(3)根据题意:铁锈是该反应的催化剂,根据催化剂的特点“一变两不变”,所以其质量和化学性质在反应前后不变,其质量仍为0.2g,步骤①的目的是与③对比,研究铁锈是否改变化学反应速率;过滤用到的仪器有铁架台、烧杯、漏斗、玻璃棒;氧化铁可与还原性物质发生反应,还可与稀盐酸或稀硫酸反应,相比之下,与酸的反应简单易行,而与还原性物质要在加热或高温条件下进行,所以可取适量固体放于试管,然后倒入稀盐酸,若固体溶解,溶液变为黄色,说明氧化铁与稀盐酸可反应;
故答案为:
质量和化学性质不变;
铁锈的质量仍为0.2 g;
与步骤③对比; 玻璃棒; 取适量固体放于试管,然后倒入稀盐酸,若固体溶解,溶液变为黄色,说明氧化铁与稀盐酸可反应.
点评:本题综合性较强,既考查了装置的选取,方程式的书写,还考查了对于催化剂概念的理解,氧化铁的化学性质等知识,能很好的考查学生对知识的理解和应用.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目