题目内容
2. 小彤的一副眼镜戴了一段时间后,发现铜质镜架上出现了一墨绿色物质,他想将其除掉.经查阅资料得知:铜在一定条件下会锈蚀生成一种绿色物质,其主要成分是碱式碳酸铜(俗称铜绿),于是他和几个同学按如下方案(如图)进行了实验.
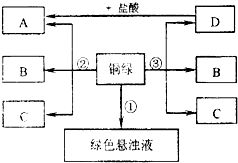
小彤的一副眼镜戴了一段时间后,发现铜质镜架上出现了一墨绿色物质,他想将其除掉.经查阅资料得知:铜在一定条件下会锈蚀生成一种绿色物质,其主要成分是碱式碳酸铜(俗称铜绿),于是他和几个同学按如下方案(如图)进行了实验.(1)实验①是向铜绿中加入适量常见无色液体B,再加热至沸,沉淀仍然不变色.实验②、③中C是一种常见的无色气体,B的化学式为H2O.为满足实验③反应所需的外界条件,应该使用关键仪器名称是酒精灯.
(2)写出实验②反应的化学方程式Cu2(OH)2CO3+4HCl═2CuCl2+3H2O+CO2↑,
在此过程中,判断铜绿没有完全反应的现象是绿色沉淀没有全部溶解.
(3)将A的溶液5~9滴滴入5mL10%的氢氧化钠溶液中得到蓝色絮状沉淀,稍加热即变黑色沉淀D.写出蓝色絮状沉淀转变为D的化学方程式Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O.
(4)已知2Ca(HCO3)═CaCO3↓+H2O+CO2↑,则热稳定性CaCO3>Ca(HCO3),由此推理上述实验中铜绿、蓝色絮状沉淀、物质D三种化合物热稳定性由强至弱的顺序是:CuO>Cu2(OH)2CO3>Cu(OH)2 (均写化学式).
(5)经过讨论.同学们建议小彤可以用盐酸除去镜架上的绿色物质.
分析 碱式碳酸铜受热分解能生成氧化铜、水和二氧化碳,和盐酸反应能生成氯化铜、水和二氧化碳;氧化铜和盐酸反应能生成氯化铜和水;氯化铜和氢氧化钠反应能生成氢氧化铜沉淀和氯化钠;氢氧化铜受热分解能生成氧化铜和水;根据反应物和生成物及其质量守恒定律可以书写化学方程式.
解答 解:(1)碱式碳酸铜受热分解能生成氧化铜、水和二氧化碳,和盐酸反应能生成氯化铜、水和二氧化碳;氧化铜和盐酸反应能生成氯化铜和水;所以C是二氧化碳,B是水.故填:H2O;酒精灯.
(2)碱式碳酸铜和盐酸反应的化学方程式为:Cu2(OH)2CO3+4HCl═2CuCl2+3H2O+CO2↑.故填:Cu2(OH)2CO3+4HCl═2CuCl2+3H2O+CO2↑;
在此过程中,判断铜绿没有完全反应的现象是绿色沉淀没有全部溶解.故填:绿色沉淀没有全部溶解.
(3)蓝色絮状沉淀是氢氧化铜,氢氧化铜受热分解能生成氧化铜和水,反应的化学方程式为:Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O.故填:Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O;
(4)由于加热氢氧化铜和碱式碳酸铜都能生成氧化铜,所以氧化铜的热稳定性强,
氢氧化铜不稳定,空气中就会失水发黑,90℃左右即开始分解为CuO;碱式碳酸铜分解温度高于100℃,空气中可以稳定存在.所以碱式碳酸铜的热稳定性比氢氧化铜的热稳定性强.
故填:CuO;Cu2(OH)2CO3;Cu(OH)2.
(5)可以用盐酸除去镜架上的绿色物质.故填:盐酸.
点评 解答本题要掌握化学方程式的书写方法和各种物质的性质等方面的知识,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
13.下列物质的用途主要由物理性质决定的是( )
| A. | 镁粉用于制作照明弹 | B. | 钨用于制作白炽灯丝 | ||
| C. | 二氧化碳用于植物的光合作用 | D. | 氮气用作焊接金属时的保护气 |
10.除去下列物质中所含少量杂质的方法不正确的是( )
| A. | 氢氧化钠中混入碳酸钠(加入足量稀盐酸) | |
| B. | FeCl2 溶液中混入CuCl2(加入足量的铁粉,过滤) | |
| C. | 一氧化碳中混入二氧化碳(将混合气体通过氢氧化钠溶液) | |
| D. | 氯化钠固体中混入碳酸钠(加入足量的稀盐酸,蒸发) |
14.某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
A.将3.0g KClO3与1.0g MnO2均匀混合加热
B.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.B中x值应取3.0
A中反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
②乙探究了影响双氧水分解速度的某种因素.实验数据记录如下
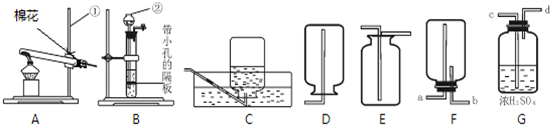
本实验中,测量O2体积的装置是图1中的C(填编号).

实验结论:在相同条件下,双氧水浓度越大双氧水分解得越快.
丙用图2装置进行实验,通过比较相同时间天平读数差值大小也能达到实验目的.
①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
A.将3.0g KClO3与1.0g MnO2均匀混合加热
B.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.B中x值应取3.0
A中反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
②乙探究了影响双氧水分解速度的某种因素.实验数据记录如下
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |

实验结论:在相同条件下,双氧水浓度越大双氧水分解得越快.
丙用图2装置进行实验,通过比较相同时间天平读数差值大小也能达到实验目的.
11.稀盐酸是化学实验中常用的试剂,但下列实验中,不宜使用稀盐酸的是( )
| A. | 除去氯化钠溶液中的碳酸钠 | B. | 除去铜粉中混有的铁粉 | ||
| C. | 除去铁粉中的氧化铁 | D. | 除去铁丝上的铁锈 |
12. 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学对该气体的成分进行如下探究.
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学对该气体的成分进行如下探究.
猜想与假设】忠旭说:该气体可能是CO2、O2、CO、H2、N2.
宇龙同学说:不可能含有N2,因为根据质量守恒定律可知,化学反应前后元素种类不变,反应物中不含氮元素;
心如同学说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒;
鸿宇同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
【得出结论】(1)由实验①可知,该气体中肯定含有二氧化碳;
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气,理由是若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃.
 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学对该气体的成分进行如下探究.
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学对该气体的成分进行如下探究.猜想与假设】忠旭说:该气体可能是CO2、O2、CO、H2、N2.
宇龙同学说:不可能含有N2,因为根据质量守恒定律可知,化学反应前后元素种类不变,反应物中不含氮元素;
心如同学说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒;
鸿宇同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气,理由是若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃.
 如图是实验室用高锰酸钾制取并收集氧气的装置,回答下列问题:
如图是实验室用高锰酸钾制取并收集氧气的装置,回答下列问题: