题目内容
5.A、B、C、D、E、F、G、H、I都是初中化学常见物质,其中B为红色固体,E、H均为黑色固体,F是一种无色气体,它们之间有如图的转化关系(部分生成物已省去).
根据转化关系图回答问题:
(1)写出A的名称氢气;
(2)写出F→E的化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.写出G→I的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O.
分析 根据A、B、C、D、E、F、G、H、I都是初中化学常见物质,B为红色固体,E、H均为黑色固体,F是一种无色气体,结合我们学过的知识,一氧化碳还原氧化铁生成铁和二氧化碳,一氧化碳还原氧化铜生成铜和二氧化碳,铜和氧气在加热的条件下反应生成氧化铜,因此B是铜,E是铁,F是一氧化碳,H是氧化铜;氧化铜和硫酸反应生成硫酸铜和水,硫酸铜和氢氧化钡反应生成硫酸钡白色沉淀和氢氧化铜蓝色沉淀,因此C是硫酸铜,D是硫酸钡和氢氧化铜的混合物;又因为一氧化碳和氧气在点燃的条件下生成二氧化碳,因此G是二氧化碳;二氧化碳能使澄清的石灰水变浑浊,因此I是碳酸钙;铁和盐酸反应生成氯化亚铁和氢气,因此A是氢气,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、D、E、F、G、H、I都是初中化学常见物质,B为红色固体,E、H均为黑色固体,F是一种无色气体,结合我们学过的知识,一氧化碳还原氧化铁生成铁和二氧化碳,一氧化碳还原氧化铜生成铜和二氧化碳,铜和氧气在加热的条件下反应生成氧化铜,因此B是铜,E是铁,F是一氧化碳,H是氧化铜;氧化铜和硫酸反应生成硫酸铜和水,硫酸铜和氢氧化钡反应生成硫酸钡白色沉淀和氢氧化铜蓝色沉淀,因此C是硫酸铜,D是硫酸钡和氢氧化铜的混合物;又因为一氧化碳和氧气在点燃的条件下生成二氧化碳,因此G是二氧化碳;二氧化碳能使澄清的石灰水变浑浊,因此I是碳酸钙;铁和盐酸反应生成氯化亚铁和氢气,因此A是氢气;
(2)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,因为G为CO2,澄清石灰水为Ca(OH)2,所以G→I的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:(1)氢气;
(2)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,CO2+Ca(OH)2=CaCO3↓+H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | 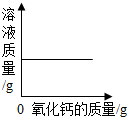 常温下,向一定量的饱和石灰水中加入氧化钙 常温下,向一定量的饱和石灰水中加入氧化钙 | |
| B. | 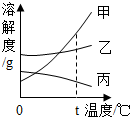 t℃时,向等质量的甲、乙、丙三种物质中分别加水配成饱和溶液,所得溶液质量最小的是丙 t℃时,向等质量的甲、乙、丙三种物质中分别加水配成饱和溶液,所得溶液质量最小的是丙 | |
| C. | 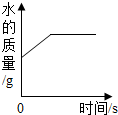 向一定质量的过氧化氢的水溶液中加入二氧化锰 向一定质量的过氧化氢的水溶液中加入二氧化锰 | |
| D. | 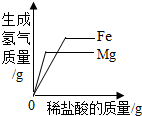 向等质量的铁和镁中分别加入足量的稀盐酸 向等质量的铁和镁中分别加入足量的稀盐酸 |
| 选项 | 事 实 | 解 释 |
| A | 炎热的夏天,自行车车胎容易爆裂 | 夏天温度高,分子间的间隔变大 |
| B | 体温计中的水银(汞)热胀冷缩 | 原子体积受热变大,遇冷变小 |
| C | 1滴水中大约有1.67×1021个水分子 | 分子很小 |
| D | 敞口容器中的酒精逐渐减少 | 分子是不断运动的 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 与足量稀盐酸充分反应,用排水法收集到VmL气体 | |
| B. | 与足量稀盐酸充分反应,称量反应后的溶液,质量为m1g | |
| C. | 与足量浓盐酸充分反应,逸出的气体用NaOH固体吸收,固体质量增加m2g | |
| D. | 与足量Ca(OH)2溶液充分反应,将沉淀过滤、洗涤、干燥,得到m3g固体 |
 如图是某化肥包装袋上的部分说明,该化肥属于( )
如图是某化肥包装袋上的部分说明,该化肥属于( )| A. | 钾肥 | B. | 氮肥 | C. | 复合肥料 | D. | 磷肥 |
| A. | 该物质含3种金属元素 | B. | 其中硅元素的化合价为+4价 | ||
| C. | 该物质由10个原子构成 | D. | 其相对分子质量为202克 |
| A. | 葡萄糖是一种无机物 | |
| B. | 天然气、氢气都属于含碳燃料 | |
| C. | 造成酸雨的主要物质是二氧化碳和二氧化硫 | |
| D. | 煤气是由一氧化碳、甲烷、氢气组成的混合物 |
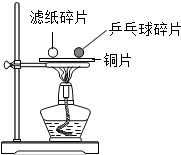 如图所示,把同样大小的滤纸碎片和乒乓球碎片分开放在一块薄铜片的两侧,加热铜片的中部,下列实验现象或结论错误的是( )
如图所示,把同样大小的滤纸碎片和乒乓球碎片分开放在一块薄铜片的两侧,加热铜片的中部,下列实验现象或结论错误的是( )| A. | 实验中使用铜片,是利用了铜的导热性 | |
| B. | 铜片受热的一面变黑,是因为产生了CuO | |
| C. | 实验过程中滤纸碎片先燃烧,乒乓球碎片后燃烧 | |
| D. | 实验说明燃烧的条件之一是温度达到可燃物的着火点 |
