题目内容
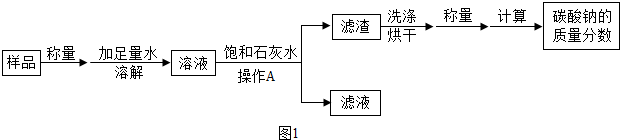
19.某天然盐碱湖泊中得到的碳酸钠产品中混有少量氯化钠,为测定该产品中碳酸钠的质量分数,甲、乙两个化学小组进行了如下探究活动.【甲组】探究活动过程如图1,请回答下列问题:
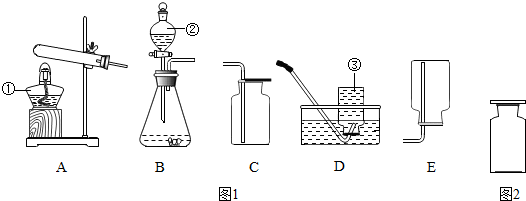
(1)操作A 用到的玻璃仪器除烧杯外,还必需有漏斗、玻璃棒;
(2)在实验过程中加入饱和石灰水后发生反应的化学方程式是:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(3)为探究上述反应后滤液中的溶质成分,甲同学向滤液中滴加过量稀盐酸,发现有气泡产生,则滴加盐酸前滤液中的溶质除氯化钠外还有碳酸钠、氢氧化钠.
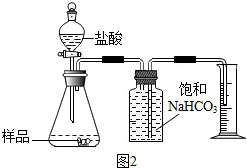
【乙组】用如图2所示装置对样品进行碳酸钠的含量分析,已知CO2在饱和NaHCO3溶液中溶解度很小.下列探究活动中的实验操作说法不正确的是BCD.
A.锥形瓶中原有的空气对实验结果无影响
B.对取用样品的量的多少无一定要求
C.实验中若改用水,对测定无影响
D.实验中加入盐酸液体的体积,对测定无影响.
分析 【甲组】(1)根据通过操作A得到了滤渣和滤液,所以操作A是过滤,以及过滤需要的玻璃仪器进行分析;
(2)根据碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠进行分析;
(3)根据碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,以及加入的碳酸钠的是过量的进行分析;
【乙组】A、根据二氧化碳在空气中的含量分析;
B、根据样品的量太多或太少对实验结果造成的影响分析;
C、根据二氧化碳在水中溶解性分析;
D、根据瓶内压强的变化分析.
解答 解:【甲组】(1)通过操作A得到了滤渣和滤液,所以操作A是过滤,过滤需要的玻璃仪器有烧杯、漏斗、玻璃棒;
(2)碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(3)碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,以及加入的碳酸钠的是过量的,所以滴加盐酸前滤液中的溶质除氯化钠外还有碳酸钠、氢氧化钠;
【乙组】A、空气中含有的二氧化碳量很少,不会对结果产生大的影响,故A正确;
B、取用样品的量产生的二氧化碳的体积不能超过量筒的体积,因为样品量太多会使液体外溢或气体外逸导致测量不准;太少会导致气体量太少,产生的气压不够,造成较大误差,故B错误;
C、由于二氧化碳能溶于水,对测定有影响,故C错误;
D、实验中加入盐酸液体的体积过多,瓶内压强增大,排除的气体较多,对测定有影响,故D错误.
故选:BCD.
故选故答案为:【甲组】(1)漏斗、玻璃棒;
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(3)碳酸钠、氢氧化钠;
【乙组】BCD.
点评 熟悉物质的性质,观察实验的装置及过程,明确实验的原理是解答本题的关键.

练习册系列答案
相关题目
9.日常生活中见到下列现象,其中发生了化学变化的是( )
| A. | 空气液化 | B. | 西瓜榨汁 | C. | 钢铁生锈 | D. | 蔗糖溶解 |
7.下列离子能在PH=11的溶液中大量共存的是( )
| A. | K+ NO3- Na+ OH- | B. | CO32- Na+ Cl- Ca2+ | ||
| C. | H+ Ba2+ Cl- SO42- | D. | K+ NO3- SO42- Cu2+ |
14.在下列各组物质中,前一种是化合物,后一种是混合物的是( )
| A. | 澄清石灰水、二氧化碳 | B. | 河水、汽水 | ||
| C. | 液氧、稀盐酸 | D. | 水蒸气、石油 |
4. 乙炔(C2H2)气体可由碳化钙固体(CaC2)与水反应生成,同时生成一种白色固体.
乙炔(C2H2)气体可由碳化钙固体(CaC2)与水反应生成,同时生成一种白色固体.
【査阅资料】Ca(OH)2与稀盐酸反应无气泡产生.
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下两种可能:
猜想一:CaC03;猜想二:Ca(0H)2
【讨论交流】做出猜想一、二的理由是:化学反应前后原子的种类及数目不变.
【进行实验】设计实验验证白色固体不是碳酸钙.
【反思与结论】猜想二正确
①写出实验室制取乙炔的化学反应方程式CaC2+2H2O=Ca(OH)2+C2H2↑.
②乙炔和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属,试写出该反应的化学方程式2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O,如图所示为氧炔焰切割机,乙炔与氧气按照2:5体积比混合点燃,焊接效果最好.
 乙炔(C2H2)气体可由碳化钙固体(CaC2)与水反应生成,同时生成一种白色固体.
乙炔(C2H2)气体可由碳化钙固体(CaC2)与水反应生成,同时生成一种白色固体.【査阅资料】Ca(OH)2与稀盐酸反应无气泡产生.
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下两种可能:
猜想一:CaC03;猜想二:Ca(0H)2
【讨论交流】做出猜想一、二的理由是:化学反应前后原子的种类及数目不变.
【进行实验】设计实验验证白色固体不是碳酸钙.
| 实验步骤 | 实验现象 | 实验结论 |
| 白色固体不是碳酸钙 |
①写出实验室制取乙炔的化学反应方程式CaC2+2H2O=Ca(OH)2+C2H2↑.
②乙炔和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属,试写出该反应的化学方程式2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O,如图所示为氧炔焰切割机,乙炔与氧气按照2:5体积比混合点燃,焊接效果最好.
11.小红用托盘天平称量10.8克(1克以下用游码)食盐,称好后发现食盐放在了右盘,则她实际称量食盐的质量是( )
| A. | 10.8克 | B. | 11.6克 | C. | 9.2克 | D. | 10克 |
8.“H-2”的说法中,正确的是 ( )
| A. | 属于一种新元素 | B. | 跟氢原子相同的原子 | ||
| C. | 是氢元素的另一种原子 | D. | 与氢元素不同类的原子 |