题目内容
19.下列各组物质的两种方法都正确的是( )| 需区分物质 | 方法一 | 方法二 |
| A.空气和氧气 | 用带火星木条检验 | 闻气味 |
| B.硬水和软水 | 观察颜色 | 加肥皂水搅拌 |
| C.铝丝和银丝 | 用磁铁吸引 | 浸入硫酸铜溶液 |
| D.氯化钠溶液和纯碱溶液 | 滴加酚酞试液 | 加入稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 鉴别不同物质时,要根据物质的不同性质进行区分,现象要明显,方法要简便;鉴别时主要通过颜色变化、是否有气泡冒出,是否有沉淀产生等现象来完成,据此结合不同物质的性质分析判断即可.
解答 解:A、空气和氧气用带火星的木条进行检验时,能使带火星木条复燃的是氧气,没有复燃的是空气,由于两者均是无味气体,所以闻气味的方式不能区分空气和氧气,不符合题意,故A错误;
B、硬水和软水颜色没有区别,一般都为无色液体,所以观察颜色不能区分硬水与软水,加入明矾只能吸附悬浮在水中不溶性杂质,也不能区分硬水和软水,不符合题意,故B错误;
C、铝丝和银丝物理性质很多不同,都不能被磁铁吸引,浸入硫酸铜溶液,铝丝表面会析出红色固体,银丝不会,不符合题意,故C错误;
D、取样品,滴入酚酞,溶液显红色的是纯碱,颜色不变的是氯化钠,可以鉴别,加入盐酸,有气泡产生的是碳酸钠,没有明显现象的是氯化钠,可以鉴别,符合题意,故D正确.
故选:D.
点评 在解此类题时,首先分析被鉴别物质的性质,然后选择适当的试剂和方法,出现不同的现象即可鉴别.

练习册系列答案
相关题目
9.粮食和人类生存发展密切相关.请根据所学的知识,回答下列问题:
(1)农作物生长过程张,需求量较大的营养元素是氮(填一种元素名称).
(2)农作物适合在中性或接近中性的土壤中生长,如果土壤呈酸性可加入适量的熟石灰来中和其酸性.
(3)请写出鉴别NH4Cl和K2SO4这两种化学肥料的实验方法、现象及实验结论:
(4)请你说出化肥过度施用产生的不良影响:会造成水体污染土壤污染和土壤板结.
(1)农作物生长过程张,需求量较大的营养元素是氮(填一种元素名称).
(2)农作物适合在中性或接近中性的土壤中生长,如果土壤呈酸性可加入适量的熟石灰来中和其酸性.
(3)请写出鉴别NH4Cl和K2SO4这两种化学肥料的实验方法、现象及实验结论:
| 实 验 方 法 | 实 验 现 象 和 结 论 |
10.下列有关资源、能源和环境的叙述正确的是( )
| A. | 氧气约占空气总质量的21%,目前空气污染指数的项目有pM2.5、臭氧等 | |
| B. | 海洋中含量最多的元素是氧,可利用的陆地淡水只约占全球水储量的2.53% | |
| C. | 核能的利用可以减缓温室效应,石油可炼制出汽油、煤油和润滑油等产品 | |
| D. | 灯丝由熔点最高的金属钛制成,合金的强度和硬度一定比组成它的纯金属高 |
7.下列实验操作正确的是( )
| A. | 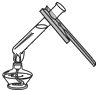 加热液体 | B. | 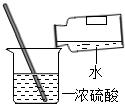 稀释浓硫酸 | C. | 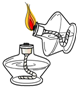 点燃酒精灯 | D. |  闻气体气味 |
14.漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,既可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,易分解生成HCl和一种常见的单质气体.HClO具有漂白性,能使品红等有色物质褪色.
【漂白粉制取的研究】
有人提出可以利用海水(含NaCl)和石灰石为原料制取漂白粉,该方法流程如图1:
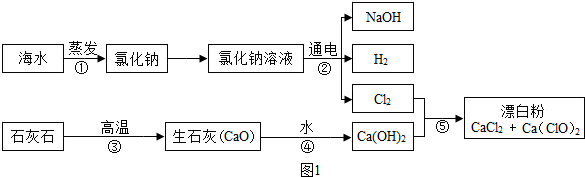
(1)⑤中的反应是2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2X,X的化学式为H2O,其中Ca(ClO)2中氯元素的化合价为+1.
(2)实际工业生产中,反应⑤的反应物Ca(OH)2最好用石灰乳,(填“饱和石灰水”或“石灰乳”)并不断搅拌.
【定性研究】
有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2 CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】
【定量研究】
已知漂白粉有效成分能与浓盐酸发生如下反应Ca(ClO)2+4HCl═CaCl2+2Cl2↑+2H2O,某同学通过查阅资料,设计一个最简单的实验,测定漂白粉有效成分的质量分数.
【资料】Cl2能溶于水,但在饱和食盐水中的溶解性非常小.实验条件下Cl2的密度为3.17g/L.
【实验探究】
(3)甲同学准确称取0.5g漂白粉样品,检查装置气密性后装入如图2A中,进行实验.实验结束后,量筒内收集到89.6mL食盐水.据此计算,此样品中有效成分的质量分数.(写出计算过程,计算过程中,保留3位小数,结果精确到0.1%)
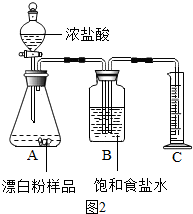
(4)在读取量筒的刻度数时,应注意①视线与凹液面最低点应齐平;②装置内气体应恢复至室温;③B、C两仪器内的液面应齐平.
(5)实验结束后,同学们发现,此装置存在着明显的不足:ABC(填序号)
A没有考虑到盐酸占据的体积对测定结果的影响.
B没有考虑到残留在导管中的液体和导管本身的体积对测定结果的影响.
C没有考虑到氯气中可能混有的二氧化碳气体对测定结果的影响
D没有考虑到氯气中可能混有的氯化氢气体对实验结果的影响.
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,易分解生成HCl和一种常见的单质气体.HClO具有漂白性,能使品红等有色物质褪色.
【漂白粉制取的研究】
有人提出可以利用海水(含NaCl)和石灰石为原料制取漂白粉,该方法流程如图1:

(1)⑤中的反应是2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2X,X的化学式为H2O,其中Ca(ClO)2中氯元素的化合价为+1.
(2)实际工业生产中,反应⑤的反应物Ca(OH)2最好用石灰乳,(填“饱和石灰水”或“石灰乳”)并不断搅拌.
【定性研究】
有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2 CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,滴加足量的稀盐酸. | 有气体产生,气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后的试管中加少量品红溶液. | 红色变浅或消失. |
已知漂白粉有效成分能与浓盐酸发生如下反应Ca(ClO)2+4HCl═CaCl2+2Cl2↑+2H2O,某同学通过查阅资料,设计一个最简单的实验,测定漂白粉有效成分的质量分数.
【资料】Cl2能溶于水,但在饱和食盐水中的溶解性非常小.实验条件下Cl2的密度为3.17g/L.
【实验探究】
(3)甲同学准确称取0.5g漂白粉样品,检查装置气密性后装入如图2A中,进行实验.实验结束后,量筒内收集到89.6mL食盐水.据此计算,此样品中有效成分的质量分数.(写出计算过程,计算过程中,保留3位小数,结果精确到0.1%)

(4)在读取量筒的刻度数时,应注意①视线与凹液面最低点应齐平;②装置内气体应恢复至室温;③B、C两仪器内的液面应齐平.
(5)实验结束后,同学们发现,此装置存在着明显的不足:ABC(填序号)
A没有考虑到盐酸占据的体积对测定结果的影响.
B没有考虑到残留在导管中的液体和导管本身的体积对测定结果的影响.
C没有考虑到氯气中可能混有的二氧化碳气体对测定结果的影响
D没有考虑到氯气中可能混有的氯化氢气体对实验结果的影响.
11.物质的性质决定其用途.下列物质的用途与性质对应关系错误的是( )
| A. | 肥皂水用于缓解蚊虫叮咬后的痛痒感----肥皂水呈弱碱性 | |
| B. | 氮气常用作保护气----常温下氮气化学性质稳定 | |
| C. | 洗洁精能洗涤油污----洗洁精能溶解油污 | |
| D. | 稀盐酸除铁锈----稀盐酸能与铁锈反应 |
 硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题:
硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题: