题目内容
(5分)普通黄铜仅由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件。为测定黄铜中铜的质量分数,取样品10 g,分四次向其中加入稀硫酸使之充分反应,实验数据记录如下表:
| | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀硫酸的质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 8.7 | 7.4 | 7 | 7 |
(1)该过程中发生反应的化学方程式为 。
(2)黄铜中铜的质量分数为 。
(3)加入的稀硫酸溶液中硫酸的质量分数是 。(写出计算过程)
(1)Zn+H2SO4=ZnSO4+H2↑ (2)70% (3)19.6%
解析试题分析:(1)根据金属活动性顺序可知,锌能与稀硫酸反应生成硫酸锌和氢气,而铜不与稀硫酸反应,故反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑ ;
(2)剩余固体质量为7g而不再减少,则样品中铜的质量为7g,黄铜中铜的质量分数=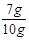 ×100%=70%;
×100%=70%;
(3)设样品中锌完全反应时,参加反应的稀硫酸溶质的质量为x,
Zn + H2SO4 ═ ZnSO4 + H2↑
65 98
10g-8.7g x
65:98=10g-8.7g:x 解得 x=1.96g;
则稀硫酸溶液中溶质的质量分数=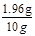 ×100%=19.6%
×100%=19.6%
答:所加入的稀硫酸的溶质质量分数19.6%。
考点:金属活动性顺序及应用;化学方程式的计算;有关溶质质量分数的计算。
点评:注意铜锌混合物中铜不与酸反应。

练习册系列答案
相关题目
普通黄铜仅由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件.为测定黄铜中铜的质量分数,取样品10g,分四次向其中加入稀硫酸使之充分反应,实验数据记录如下表:
认真分析数据,回答下列问题:
(1)黄铜中铜的质量分数为
(2)恰好完全反应时,溶液中溶质的质量分数是.
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀硫酸的质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 8.7 | 7.4 | 7 | 7 |
(1)黄铜中铜的质量分数为
(2)恰好完全反应时,溶液中溶质的质量分数是.
普通黄铜仅由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件.为测定黄铜中铜的质量分数,取样品10g,分四次向其中加入稀硫酸使之充分反应,实验数据记录如下表:
认真分析数据,回答下列问题:
(1)该过程中发生反应的化学方程式为 .
(2)黄铜中铜的质量分数为 .
(3)求所加入的稀硫酸的溶质质量分数.
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀硫酸的质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 8.7 | 7.4 | 7 | 7 |
(1)该过程中发生反应的化学方程式为
(2)黄铜中铜的质量分数为
(3)求所加入的稀硫酸的溶质质量分数.
普通黄铜仅由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件.为测定黄铜中铜的质量分数,取样品10g,分四次向其中加入稀硫酸使之充分反应,实验数据记录如下表:
认真分析数据,回答下列问题:
(1)该过程中发生反应的化学方程式为______.
(2)黄铜中铜的质量分数为______.
(3)求所加入的稀硫酸的溶质质量分数.
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀硫酸的质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 8.7 | 7.4 | 7 | 7 |
(1)该过程中发生反应的化学方程式为______.
(2)黄铜中铜的质量分数为______.
(3)求所加入的稀硫酸的溶质质量分数.