题目内容
 右图为实验室保存的一瓶过氧化氢溶液的标签.某小组同学利用该溶液加水配成6%过氧化氢溶液100g,用来制取氧气.
右图为实验室保存的一瓶过氧化氢溶液的标签.某小组同学利用该溶液加水配成6%过氧化氢溶液100g,用来制取氧气.
试分析计算:
(1)在配制6%过氧化氢溶液过程中需水______毫升;
(2)H2O2中氢元素和氧元素的质量比为______;
(3)68克6%的过氧化氢溶液中含______克氢元素(保留两位小数).
解:(1)设需要过氧化氢溶液的质量为x,
x×30%=100g×6%
x=20g,
所以加入水的质量为100g-20g=80g
水的密度是1g/mL,所以水的体积是80mL,
故答案为:80;
(2)氢元素和氧元素的质量比=(2×1):(2×16)=1:16,故答案为:1:16;
(3)氢元素质量:68×6%× +68×94%×
+68×94%×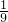 =7.34g,故答案为:7.34.
=7.34g,故答案为:7.34.
分析:(1)根据溶液稀释前后的溶质质量不变进行分析;
(2)根据化学式和相对原子质量进行分析;
(3)根据元素质量的解法进行分析.
点评:在解此类题时,首先分析题中考查的问题,然后结合题中的数据和学过的知识进行分析解答.
x×30%=100g×6%
x=20g,
所以加入水的质量为100g-20g=80g
水的密度是1g/mL,所以水的体积是80mL,
故答案为:80;
(2)氢元素和氧元素的质量比=(2×1):(2×16)=1:16,故答案为:1:16;
(3)氢元素质量:68×6%×
 +68×94%×
+68×94%×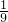 =7.34g,故答案为:7.34.
=7.34g,故答案为:7.34.分析:(1)根据溶液稀释前后的溶质质量不变进行分析;
(2)根据化学式和相对原子质量进行分析;
(3)根据元素质量的解法进行分析.
点评:在解此类题时,首先分析题中考查的问题,然后结合题中的数据和学过的知识进行分析解答.

练习册系列答案
相关题目
 过氧化氢溶液在存放过程中会缓慢分解.右图为实验室保存的一瓶过氧化氢溶液的标签.某小组同学为了解过氧化氢的分解情况,取5g该溶液共制得0.64g氧气.试分析计算
过氧化氢溶液在存放过程中会缓慢分解.右图为实验室保存的一瓶过氧化氢溶液的标签.某小组同学为了解过氧化氢的分解情况,取5g该溶液共制得0.64g氧气.试分析计算

