题目内容
18.亚硝酸钠(NaNO2)有良好的防腐作用,常用作肉类食品的添加剂,但亚硝酸钠有毒,过量食用会中毒,因而用量严格限制.以下为亚硝酸钠的一些性质:A.水溶液呈碱性 B.暴露在空气中易于氧气反应生成硝酸钠
C.加热至220℃以上会分解出红棕色、有刺激性气味、有毒的气体.
请根据以上信心回答:
(1)亚硝酸钠保存时要注意避免高温和密封.
(2)请你设局一种鉴别NaNO2和NaCl的方法,写出简单的操作过程、现象和结论:分别取样加水溶解,向其中滴加酚酞试液,若酚酞试液变红色,说明原物质是亚硝酸钠,若酚酞试液不变色,说明原物质是氯化钠.
(3)NaNO2中氮元素的化合价为+3,写出性质B的化学方程式:2NaNO2+O2═2NaNO3.
分析 (1)根据亚硝酸钠的性质可以判断保存的方法;
(2)亚硝酸钠溶液显碱性,能使酚酞试液变红色,氯化钠溶液显中性,不能使酚酞试液变色;
(3)化合物中元素的化合价代数和为零;
根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
解答 解:(1)因为亚硝酸钠加热至220℃以上会分解,因此保存亚硝酸钠时应该避免高温;
因为亚硝酸钠暴露在空气中易与氧气反应生成硝酸钠,因此保存亚硝酸钠时应该密封.
故填:避免高温;密封.
(2)鉴别NaNO2和NaCl的方法是:分别取样加水溶解,向其中滴加酚酞试液,若酚酞试液变红色,说明原物质是亚硝酸钠,若酚酞试液不变色,说明原物质是氯化钠.
故填:分别取样加水溶解,向其中滴加酚酞试液,若酚酞试液变红色,说明原物质是亚硝酸钠,若酚酞试液不变色,说明原物质是氯化钠.
(3)设NaNO2中氮元素的化合价为x,
NaNO2中,钠元素的化合价是+1,氧元素的化合价是-2,
根据题意有:(+1)+x+(-2)×2=0,
x=+3,
亚硝酸钠和氧气反应的化学方程式为:2NaNO2+O2═2NaNO3.
故填:=+3;2NaNO2+O2═2NaNO3.
点评 鉴别NaNO2和NaCl时,也可以利用加热的方法鉴别,因为亚硝酸钠加热到220℃以上会分解出红棕色、有刺激性气味、有毒的气体,而氯化钠在该温度下不能分解.

练习册系列答案
相关题目
8.下列变化中没有新物质生成的是( )
| A. | 燃放烟花 | B. | 干冰升华 | C. | 食物腐烂 | D. | 燃煤发电 |
9.下列反应中属于中和反应的是( )
| A. | Ca(OH)2+CO2═CaCO3+H2O | B. | 6HCl+Fe2O3═2FeCl3+3H2O | ||
| C. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | D. | NaOH+HNO3═NaNO3+H2O |
6.对下列现象的解释或者结论错误的是( )
| A. | “花香四溢”--分子在不断运动 | |
| B. | 过氧化氢分解--在化学变化中分子可以再分 | |
| C. | 铁制品表面刷漆--可防止生锈 | |
| D. | 伸入集气瓶中燃着的木条熄灭--瓶中气体一定是CO2 |
13.鉴别下列各组物质所用方法或试剂(在括号内)不正确的是( )
| A. | 棉线和羊毛线(点燃,闻气味) | B. | 过磷酸钙和氯化铵(观察颜色) | ||
| C. | 氧化铜粉末和铁粉(稀硫酸) | D. | 氢氧化钠溶液和石灰水(稀盐酸) |
7.实验室有一瓶碳酸钠和氯化钠组成的混合溶液,现要测定碳酸钠和氯化钠的质量分数,为此设计并进行了如下实验:
【实验1】取该混合液200g,向其中逐滴加入稀盐酸,当加入稀盐酸的质量为20g、40g、60g 时,生成气体的质量见下表(气体的溶解度忽略不计).
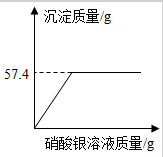
【实验2】另取该溶液200g,加入一定量稀盐酸充分反应后,测得溶液的pH=7,然后再加入硝酸银溶液,测得实验数据见图,
试分析计算:
(1)【实验1】中,第一组数据m为2.0g.
(2)混合液中碳酸钠的质量分数是多少?(计算结果精确至0.1%)
【实验1】取该混合液200g,向其中逐滴加入稀盐酸,当加入稀盐酸的质量为20g、40g、60g 时,生成气体的质量见下表(气体的溶解度忽略不计).
【实验2】另取该溶液200g,加入一定量稀盐酸充分反应后,测得溶液的pH=7,然后再加入硝酸银溶液,测得实验数据见图,
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 稀盐酸的质量/g | 20 | 40 | 60 |
| 生成气体的质量/g | m | 4.0 | 4.4 |
(1)【实验1】中,第一组数据m为2.0g.
(2)混合液中碳酸钠的质量分数是多少?(计算结果精确至0.1%)
