题目内容
17.除去下列各物质中的少量杂质,所选用的试剂、方法均正确的是( )| 物质 | 杂质(少量) | 加入试剂及用量 | 除杂操作方法 | |
| A | KCl溶液 | CaCl2 | 适量的Na2CO3溶液 | 过滤,除去滤渣 |
| B | NaOH | Na2CO3 | 过量的盐酸 | 加热蒸发 |
| C | Cu(NO3)2 | AgNO3 | 过量的铜粉 | 过滤 |
| D | CO | CO2 | 足量的氧化铜 | 加热 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CaCl2能与适量的Na2CO3溶液反应生成碳酸钙沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钠,不符合除杂原则,故选项所采取的方法错误.
B、Na2CO3和NaOH均能与过量的盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、CO能与足量的氧化铜反应生成铜和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
7.下列的实验现象的描述中正确的是( )
| A. | 木炭在氧气中燃烧比空气更旺,产生明亮的黄色火焰,放出大量的热,生成二氧化碳 | |
| B. | 磷在空气中燃烧产生大量的白雾,生成白色固体 | |
| C. | 硫在氧气中燃烧产生明亮的蓝紫色火焰,产生刺激性气味的气体 | |
| D. | 细铁丝在空气中剧烈燃烧,火星四射,放出大量的热,生成黑色固体 |
8.下列公共标志与消防安全无关的是( )


| A. | ①② | B. | ②③ | C. | ③④ | D. | ③④⑤ |
5.下列有关质量守恒定律的理解,正确的是( )
| A. | 5g铁和5g铜混合,物质的总质量为10g,遵守质量守恒定律 | |
| B. | 化学反应前后分子的总数一定不会发生改变 | |
| C. | 5g硫和5g氧气完全反应,生成物质量为10g,遵守质量守恒定律 | |
| D. | 镁条燃烧后质量增加,未遵守质量守恒定律 |
2.下列方法不能将二氧化碳气体和一氧化碳气体区分开的是( )
| A. | 分别插入燃着的木条;观察现象 | |
| B. | 分别通入碳酸钠溶液中;观察现象 | |
| C. | 分别通入紫色石蕊试液中;观察现象 | |
| D. | 分别通过灼热的氧化铜;观察现象 |
9.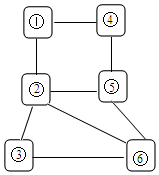 如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )
如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )
 如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )
如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| A | CO2 | NaOH | HCl | Ca(OH)2 | CuCl2 | Fe |
| B | CaO | HCl | Fe | H2SO4 | Na2CO3 | Ca(OH)2 |
| C | Fe | H2SO4 | BaCl2 | Cu(NO3)2 | Ca(OH)2 | Na2CO3 |
| D | Zn | HCl | CaCO3 | CuSO4 | NaOH | FeCl3 |
| A. | A | B. | B | C. | C | D. | D |
8. 菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究.取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:
菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究.取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:
说明:菱镁矿中的杂质不溶于水,不与酸发生反应.
(1)10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为4.4g.
(2)计算该菱镁矿中镁元素的质量分数.(写出计算过程)
(3)该实验研究中所用H2SO4溶液的溶质的质量分数是9.8%.
(4)为避免溶液排放对环境的影响,某同学对上述反应后溶液进行了过滤,并在滤液中加入了l.71%的Ba(OH)2溶液.请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图.(在答题卡的坐标中作图,并标出曲线折点的坐标)
 菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究.取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:
菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究.取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:| 加入H2SO4溶液的质量/g | 50 | 100 | 150 | 200 |
| NaOH溶液增加的质量/g | 2.2 | 4.4 | 4.4 | 4.4 |
(1)10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为4.4g.
(2)计算该菱镁矿中镁元素的质量分数.(写出计算过程)
(3)该实验研究中所用H2SO4溶液的溶质的质量分数是9.8%.
(4)为避免溶液排放对环境的影响,某同学对上述反应后溶液进行了过滤,并在滤液中加入了l.71%的Ba(OH)2溶液.请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图.(在答题卡的坐标中作图,并标出曲线折点的坐标)
