题目内容
一定质量的锌与100g稀硫酸恰好完全反应,生成0.2g氢气.计算稀硫酸中溶质的质量分数是多少?
【答案】分析:根据锌与硫酸反应的方程式,由氢气的质量可以求硫酸的质量,再根据溶质的质量分数公式求稀硫酸中溶质的质量分数.
解答:解:设硫酸的质量为x
Zn+H2SO4=ZnSO4+H2↑
98 2
x 0.2g
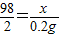 解得:x=9.8g
解得:x=9.8g
稀硫酸中溶质的质量分数是: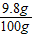 ×100%=9.8%
×100%=9.8%
答:稀硫酸中溶质的质量分数是9.8%.
点评:做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,还要记牢质量分数的公式.本考点主要出现在计算题中.
解答:解:设硫酸的质量为x
Zn+H2SO4=ZnSO4+H2↑
98 2
x 0.2g
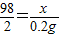 解得:x=9.8g
解得:x=9.8g稀硫酸中溶质的质量分数是:
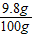 ×100%=9.8%
×100%=9.8%答:稀硫酸中溶质的质量分数是9.8%.
点评:做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,还要记牢质量分数的公式.本考点主要出现在计算题中.

练习册系列答案
相关题目
