题目内容
现有实验药品:一定质量的锌(片状或粒状)、浓硫酸和水.如上图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0~100 mL),B、C管可固定在铁架台上,供量气用;C管可上下移动,以调节液面高低.利用此装置将锌与稀硫酸反应可测定锌的相对原子质量(设锌全部反应,产生的气体不超过50 mL).

(1)实验前应如何检查装置的气密性?
______________________________.
(2)①按图示装置实验,要保证不漏出氢气,应如何操作?
______________________________;
②若改变气体发生装置,但仍要求保证不漏气,在中学的常用仪器中,可选用________等仪器来装配及完成该实验.
(3)为了较准确地测量氢气的体积,实验时应①恢复到室温;②________;③在读取反应前后B管中液面的读数时应________.
答案:
解析:
解析:
|
(1)在C管中注入适量的水,使C管液面高于B管液面,静止片刻,观察,若水面保持不变,则说明装置气密性良好.(其他合理答案也可) (2)①取下试管A,向其中加入适量的水,再沿试管壁慢慢加入少量浓H2SO4,振荡,使液体总体积不超过试管容积的1/3,将试管斜放,把锌片放在试管内壁上,塞紧塞子,慢慢直立,使锌片滑下与稀H2SO4接触.②100 mL烧瓶、带分液漏斗和导管的双孔塞、烧杯及玻璃棒 (3)调节B、C两管液面高度至相平 注意视线与凹液面最低处相平 |

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
 17、现有实验药品:一定质量的锌 (片状或粒状)、浓硫酸和水.如右图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架台上,供量气用;C管可上下移动,以调节液面高低.利用此装置将锌与稀硫酸反应可测定锌的相对原子质量(设锌全部反应,产生的气体不超过50mL).
17、现有实验药品:一定质量的锌 (片状或粒状)、浓硫酸和水.如右图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架台上,供量气用;C管可上下移动,以调节液面高低.利用此装置将锌与稀硫酸反应可测定锌的相对原子质量(设锌全部反应,产生的气体不超过50mL).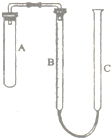 现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL).
现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL). 现有实验药品:一定质量的锌 (片状或粒状)、浓硫酸和水.如右图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架台上,供量气用;C管可上下移动,以调节液面高低.利用此装置将锌与稀硫酸反应可测定锌的相对原子质量(设锌全部反应,产生的气体不超过50mL).
现有实验药品:一定质量的锌 (片状或粒状)、浓硫酸和水.如右图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架台上,供量气用;C管可上下移动,以调节液面高低.利用此装置将锌与稀硫酸反应可测定锌的相对原子质量(设锌全部反应,产生的气体不超过50mL).
