题目内容
15.有一包固体混合物,其中含硝酸钠和某一不溶性杂质.将其投入一定量的水中,使其充分溶解,所得结果如表:| 温度/℃ | 10 | 40 | 75 |
| 剩余物质的质量(克) | 201 | 132 | 72 |
| 温度/℃ | 10 | 25 | 40 | 50 | 55 | 60 | 65 | 75 | 80 |
| 溶解度/g | 81 | 92 | 104 | 114 | 117 | 124 | 130 | 150 | 166 |
(2)原固体混合物中含多少克硝酸钠?
(3)欲完全溶解原固体混合物中的硝酸钠,所需最低温度为多少?
分析 (1)根据升温后又溶解的硝酸钠的质量和升温后溶解度增加的质量进行分析即可;(2)根据升温到75℃时的溶解度变化可知,现在硝酸钠已经全部溶解完,72g全部是杂质,再根据10℃溶解的硝酸钠质量加上升温后溶解的硝酸钠的质量即可;(3)结合溶解质量和硝酸钠溶质的质量进行分析.
解答 解:(1)根据40℃剩余物质132g,再升温到75℃,剩余物质又少了,说明升温到40℃时,固体中还含有硝酸钠;该物质由10℃升温到40℃,又溶解了201g-132g=69g,由10℃升温到40℃硝酸钠的溶解度增加了104g-81g=23g,即100g水中能多溶解23g,又因为升温后溶解了69g,所以水的质量300g;
(2)40℃升温到75℃时的溶解度增加了150g-104g=46g,所以300g水中还能溶解3×46g=138g,但实际溶解了132g-72g=60g,说明硝酸钠已经全部溶解完,所以72g全部是杂质,由10℃升温到75℃,共溶解硝酸钠质量为201g-72g=129g,10℃溶解硝酸钠质量为3×81g=243g;所以原固体混合物中含有硝酸钠的总质量为:129g+243g=372g;
(3)300g水中溶解372g硝酸钠,则100g水中溶解硝酸钠质量为124g,由溶解度表可知所需最低温度为60℃.
故答案为:(1)300;(2)372;(3)60℃.
点评 解答本题关键是要知道升温后又溶解了多少溶质,升温后溶解度的变化情况分析出原来溶液中溶剂的质量,再进一步进行分析即可.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
6.分类是学习和研究化学的常用方法.下列分类中正确的是( )
| A. | 有机物:甲烷、乙醇、乙酸 | |
| B. | 复合肥料:尿素[CO(NH2)2]、硝酸钾、磷酸氢二铵[NH4H2PO4] | |
| C. | 混合物:煤、石油、冰水共存物 | |
| D. | 合成材料:合金、合成橡胶、合成纤维 |
10.将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下.下列说法正确的是( )
| 物 质 | a | b | c | d |
| 反应前质量/g | 6.40 | 3.20 | 4.00 | 0.50 |
| 反应后质量/g | 待测 | 2.56 | 7.20 | 0.50 |
| A. | a和b是反应物,d一定是催化剂 | |
| B. | 反应后a物质的质量为4.64g | |
| C. | c物质中元素的种类,一定和a、b二种物质中元素的种类相同 | |
| D. | 若物质a与b的相对分子质量之比为2:1,则反应中a与b的化学计量数之比为4:1 |
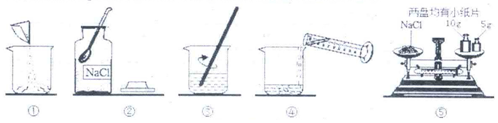
4.配置一定质量分数的食盐溶液,会引起食盐质量分数偏小的操作是( )
| A. | 称量完固体食盐时,天平指针向左倾斜 | |
| B. | 用量筒取水时,俯视读数 | |
| C. | 用量筒取水时,仰视读数 | |
| D. | 取已配置好的食盐溶液时,有少量溶液洒在瓶外 |
5.今年春季,我国西南地区发生了百年一遇的特大旱灾,国家投入大量人力物力来保障灾区人民的基本生活用水.下列关于水的认识正确的是( )
| A. | 长江、黄河发源的地区水循环比森林覆盖良好的水库区的水循环要活跃 | |
| B. | 水是良好的溶剂,许多物质都能溶于水 | |
| C. | 为补充西南地区的水资源,可以大范围地改变水循环的环节,如改变水汽输送 | |
| D. | 蒸馏水是纯净水,不含杂质,长期饮用对人体有益 |