题目内容
11.碳酸钡广泛应用于显像管(CRT)、陶瓷、光学玻璃等行业.有一种碳酸盐矿石其主要成分为碳酸钡和碳酸钙,以此矿石为原料生产碳酸钡的流程如图所示.
【已知】:碳酸钡和碳酸钙具有相似的化学性质,高温下能分解成两种氧化物;氧化钡和氧化钙都能与水反应生成对应的氢氧化物,这两种氢氧化物均可以和二氧化碳反应.但氢氧化物溶解度有一定的差异,下表所示的是两种氢氧化物在不同温度下的溶解度.
| 温度/℃ | 0 | 40 | 80 |
| Ca(OH)2溶解度/g | 0.187 | 0.141 | 0.094 |
| Ba(OH)2溶解度/g | 1.67 | 8.22 | 101.4 |
(2)以下相关说法正确的是AC.
A.焙烧炉中添加焦炭粉和热空气是为了维持炉内的高温状态
B.焙烧炉内只涉及分解反应
C.废渣需要经过洗涤才能弃渣,是为了保护环境,同时充分利用原料
(3)写出焙烧炉中含钡元素物质发生反应的化学方程式:BaCO3$\frac{\underline{\;高温\;}}{\;}$BaO+CO2↑;
(4)除了水之外,进入分离池中的物质是Ba(OH)2和Ca(OH)2,请你推测分离池中操作②的方法是B(选填“A”或“B”). A.降温,过滤; B.加热,过滤
(5)写出由溶液B制取产品的化学方程式:Ba(OH)2+CO2=BaCO3↓+H2O;
(6)若此矿石原料50t,得到的产品质量为19.7t,则此矿石中钡元素的质量分数27.4%(写出计算过程)
分析 本题是酸碱盐的应用中的物质的制备,由题目给出的信息可知:
(1)考虑增大接触面积,充分反应;
(2)焙烧炉中添加焦炭粉和热空气是为了维持炉内的高温状态是正确的;废渣需要经过洗涤才能弃渣,是为了保护环境,同时充分利用原料是正确的;焙烧炉内涉及分解反应和化合反应,因此C是错误的.(3)焙烧炉中碳酸钡在高温的条件下生成氧化钡和二氧化碳,碳酸钙在高温的条件下生成氧化钙和二氧化碳;
(4)氧化钡和水反应生成氢氧化钡,氧化钙和水反应生成氢氧化钙;因此除了水之外,进入分离池中的物质是氢氧化钡和氢氧化钙;分离池中操作②的方法是:升温、过滤,因为氢氧化钙的溶解度随温度的升高而减小;
(5)由溶液B制取产品是二氧化碳与氢氧化钡反应生成碳酸钡白色沉淀和水;
(6)根据化学式、元素的质量分数,写出计算过程.
解答 解:(1)矿石研磨成粉末的目的增大接触面积,充分反应
(2)焙烧炉中添加焦炭粉和热空气是为了维持炉内的高温状态是正确的;废渣需要经过洗涤才能弃渣,是为了保护环境,同时充分利用原料是正确的;焙烧炉内涉及分解反应和化合反应,因此C是错误的;故答案为:AC;
(3)焙烧炉中碳酸钡在高温的条件下生成氧化钡和二氧化碳,故答案为:BaCO3$\frac{\underline{\;高温\;}}{\;}$BaO+CO2↑;
(4)氧化钡和水反应生成氢氧化钡,氧化钙和水反应生成氢氧化钙;因此除了水之外,进入分离池中的物质是氢氧化钡和氢氧化钙;分离池中操作②的方法是:升温、过滤,因为氢氧化钙的溶解度随温度的升高而减小;故答案为:Ba(OH)2、Ca(OH)2,B.
(5)由溶液B制取产品是二氧化碳与氢氧化钡反应生成碳酸钡白色沉淀和水,故答案为:Ba(OH)2+CO2=BaCO3↓+H2O;
(6)因为得到的产品碳酸钡的质量为19.7t,故矿石中钡元素的质量为19.7t×$\frac{137}{137+12+16×3}×100%$=13.7t,故此矿石中钡元素的质量分数为$\frac{13.7t}{50t}×100%$=27.4%
故答案为:
(1)增大接触面积,充分反应; (2)AC
(3)BaCO3$\frac{\underline{\;高温\;}}{\;}$BaO+CO2↑;(4)Ba(OH)2、Ca(OH)2,B;
(5)Ba(OH)2+CO2=BaCO3↓+H2O; (6)27.4%
点评 本考点属于实验题中的物质的制备题,综合性比较强,需要掌握酸碱盐的性质,还要掌握相互之间的反应规律和反应的条件.还要注意根据题目给出的信息判断属于哪一种类型,各有什么注意事项,要把握好.本考点主要出现在实验题中.

 阅读快车系列答案
阅读快车系列答案| 序号 | 物质 | 杂质(少量) | 试剂和操作方法 |
| A | O2 | H2O | 通过浓H2SO4,洗气 |
| B | 稀盐酸 | 稀硫酸 | 加入过量BaCl2溶液,过滤 |
| C | CaO粉末 | CaCO3粉末 | 加入稀盐酸 |
| D | NaOH溶液 | Na2CO3溶液 | 加入适量的CaCl2溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
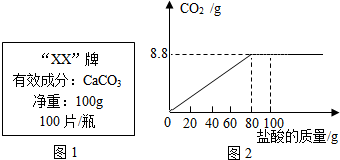 钙是人体中的常量元素,缺钙时可通过使用保健药剂来增加摄入量,某补钙药剂说明书的部分信息如图所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不参与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题.
钙是人体中的常量元素,缺钙时可通过使用保健药剂来增加摄入量,某补钙药剂说明书的部分信息如图所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不参与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题. | 第1次 | 第3次 | 第4次 | 第5次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | a | 20 | 20 |
(2)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).
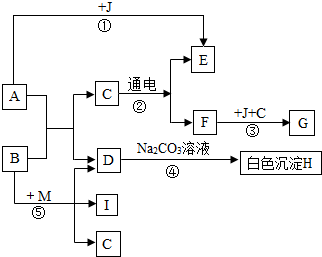 框图中A是人体胃液中含有的成分,B用于改良酸性土壤,M是一种氮肥.G是铁锈的主要成分(Fe2O3•xH2O),E、F、I为无色气体.根据图示回答下列问题.
框图中A是人体胃液中含有的成分,B用于改良酸性土壤,M是一种氮肥.G是铁锈的主要成分(Fe2O3•xH2O),E、F、I为无色气体.根据图示回答下列问题.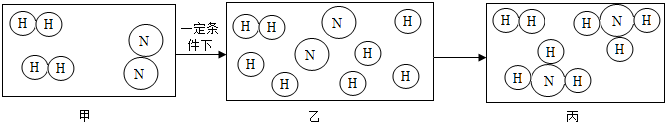 (1)请你将甲图补充完整;
(1)请你将甲图补充完整; 某实验小组的同学正在进行碳酸钠与稀盐酸反应的探究实验(如图),请回答问题:
某实验小组的同学正在进行碳酸钠与稀盐酸反应的探究实验(如图),请回答问题: