题目内容
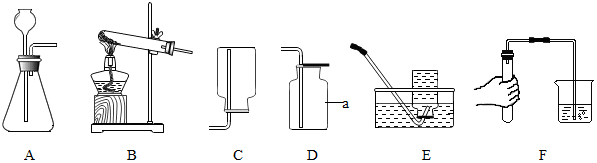
6.(1)如图是探究质量守恒的实验装置,锥形瓶内插有一根上端系有小气球,下端能与白磷接触的玻璃管,引燃白磷,气球胀大,待锥形瓶冷却到室温后,气球部分缩进玻璃管内,气球缩进的原因是氧气消耗,导致锥形瓶中的气压减小,若把玻璃管换成玻璃棒,在实验过程中可能会产生什么样的后果瓶塞飞出.
(2)小明同学学了质量守恒定律后,自己查资料得知铁粉和稀硫酸在常温下可反应生成硫酸亚铁和氢气,于是他设计了如图所示的实验,探究物质发生化学变化的前后,总质量是否发生了改变?请你和小明按下面的过程一起探究:
①提出假设:物质发生化学变化后,总质量不变(填“变”或“不变”)
②设计实验方案:按你的假设小明设计了如图装置的实验,实验进行时把气球中的铁粉倒入稀硫酸中,此反应的化学方程式为Fe+H2SO4═FeSO4+H2↑;反应后,你认为天平最终能平衡吗?说出你的理由不能平衡,这是因为反应生成的氢气使气球膨胀,产生向上的浮力.
分析 化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和;
化学反应前后,元素的种类不变,原子的种类、总个数和质量不变.
解答 解:(1)待锥形瓶冷却到室温后,气球部分缩进玻璃管内,气球缩进的原因是氧气消耗,导致锥形瓶中的气压减小;
若把玻璃管换成玻璃棒,在实验过程中,由于放热导致锥形瓶中气压增大,可能会导致瓶塞飞出.
故填:氧气消耗,导致锥形瓶中的气压减小;瓶塞飞出.
(2)①提出假设:物质发生化学变化后,总质量不变.
故填:不变.
②实验进行时把气球中的铁粉倒入稀硫酸中,铁和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑;
反应后天平最终不能平衡,这是因为反应生成的氢气使气球膨胀,产生向上的浮力.
故填:Fe+H2SO4═FeSO4+H2↑;不能平衡,这是因为反应生成的氢气使气球膨胀,产生向上的浮力.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
相关题目
9.下列有关物质的用途的说法,正确的是( )
| A. | 用苛性钠中和土壤的酸性 | B. | 用小苏打中和过多胃酸 | ||
| C. | 硫酸铜可用于配制农药波尔多液 | D. | 消石灰不能用于树木防虫 |
16.呼气是人体散失水分的途径之一,下列实例中,不能证明这一点的是( )
| A. | 冬天气温很低时,一边说话一边会冒出“白气” | |
| B. | 向澄清的石灰水吹气,石灰水会变浑浊 | |
| C. | 口罩戴的时间长了会很潮湿 | |
| D. | 擦玻璃时,朝玻璃呵几下气,可以擦得干净些 |

 往盛有一定量CaCl2溶液的烧杯中缓慢加入Na2CO3溶液,充分反应,测得如图所示的烧杯中溶液总质量随加入的Na2CO3溶液质量的变化图象.(注:CaCl2溶液显中性)
往盛有一定量CaCl2溶液的烧杯中缓慢加入Na2CO3溶液,充分反应,测得如图所示的烧杯中溶液总质量随加入的Na2CO3溶液质量的变化图象.(注:CaCl2溶液显中性)
