题目内容
14.维生素C,又叫抗坏血酸,已知该物质的化学式为C6H8O6,试计算:(1)该分子中碳、氢、氧的原子个数比为3:4:3.
(2)该物质中碳、氧元素的质量比为3:4.
(3)17.6克该物质所含氧元素的质量是多少?9.6g.
分析 (1)根据一个维生素C分子的构成进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)一个维生素C分子是由6个碳原子、8个氢原子和6个氧原子构成的,则该分子中碳、氢、氧的原子个数比为6:8:6=3:4:3.
(2)维生素C中碳元素、氧元素的质量比为 (12×6):(16×6)=3:4.
(3)17.6克该物质所含氧元素的质量是17.6g×$\frac{16×6}{12×6+1×8+16×6}×$100%=9.6g.
故答案为:(1)3:4:3;(2)3:4;(3)9.6g.
点评 本题难度不大,考查同学们灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
5.“神七”载人飞船所用固体燃料是铝粉和高氯酸铵的混合物,发射时,点燃铝粉产生大量的热引发高氯酸铵发生如下反应:2NH4ClO4 $\frac{\underline{\;高温\;}}{\;}$N2↑+2O2↑+Cl2↑+4X↑,则气体X的化学式为( )
| A. | H2O | B. | NO | C. | HCl | D. | NH3 |
2.建立宏观和微观之间的联系是化学学科特有的思维方式.下列对宏观事实的微观解释错误的是( )
| A. | 缉毒犬能根据气味发现毒品,是因为分子在不断运动 | |
| B. | 10mL酒精和10mL 水混合后体积小于20mL,是因为分子变小了 | |
| C. | 不同酸的化学性质有所不同,是因为解离生成的酸根离子不同 | |
| D. | 水电解生成氢气和氧气,是因为分子在化学变化中可以改变 |
3.20℃,取四份一定质量的饱和硝酸钾溶液进行如下实验后,所得结论正确的是( )
| A. | 保持温度不变,减少10g溶剂后,溶液中溶质的质量分数增大 | |
| B. | 保持温度不变,加入10g溶剂后,溶液中溶质的质量分数增大 | |
| C. | 保持温度不变,加入10g溶剂后,溶质的溶解度减小 | |
| D. | 降温至10℃后,溶质的溶解度减小 |
4.下列实验操作正确的是( )
| A. |  称取氢氧化钠固体 | B. |  加热液体 | ||
| C. |  取用液体 | D. |  读出液体的体积 |
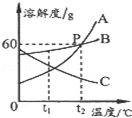 如图为A、B、C三种固体物质的溶解度曲线,根据图示完成问题:
如图为A、B、C三种固体物质的溶解度曲线,根据图示完成问题: