题目内容
9.有7种白色粉末:CuSO4、NaCl、NaOH、Na2CO3、CaO、CaCO3、Ca(OH)2.现从其中的两种物质中各取少量混合在一起,并进行如下实验.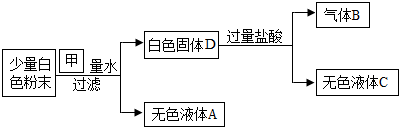
回答下列问题:
(1)写出生成气体B的化学式CO2.
(2)当甲为“足量”,白色固体D的化学式为CaCO3.若将无色液体A、C混合后的溶液蒸干,得到的混合粉末的可能组成是氢氧化钙、氯化钙或氢氧化钠、氯化钙;若无色液体A的pH=7时,该混合粉末的可能是NaCl、CaCO3;若无色液体A中含有两种溶质,这两种溶质可能是NaCl、NaOH.
(3)若甲为“一定量”,无色液体C中有两种溶质,则白色固体D中可能物质组合有碳酸钠或碳酸钙.
分析 根据粉末溶于水,得到无色液体A,因为硫酸铜溶液是蓝色的,所以一定不含有硫酸铜;白色沉淀可能是原有的碳酸钙产生的,也可能是碳酸钠和氢氧化钙反应产生的碳酸钙沉淀,但白色沉淀一定是碳酸钙;碳酸钙和过量的盐酸反应产生二氧化碳气体和氯化钙,因此无色滤液中一定含有生成的氯化钙和过量的盐酸等知识进行分析.
解答 解:粉末溶于水,得到无色液体A,因为硫酸铜溶液是蓝色的,则一定不含有硫酸铜;白色沉淀可能是原有的碳酸钙产生的,也可能是碳酸钠和氢氧化钙反应产生的碳酸钙沉淀,但白色沉淀一定是碳酸钙;碳酸钙和过量的盐酸反应产生二氧化碳气体和氯化钙,因此无色滤液中一定含有生成的氯化钙和过量的盐酸,
(1)生成气体B的化学式是:CO2;
(2)当水为“足量”,只有碳酸钙难溶于水,所以白色固体D的化学式为:CaCO3,碳酸钙可能是氢氧化钙和碳酸钠生成的,碳酸钠和氢氧化钙反应可能刚好完全反应,也可能氢氧化钙过量或碳酸钠过量,碳酸钠和氯化钙不能共存,也可能是原来就有的,碳酸钙和盐酸反应生成氯化钙,所以得到的混合粉末的可能组成是氢氧化钙、氯化钙或氢氧化钠、氯化钙,所以若无色液体A的pH=7时,该混合粉末的可能是:NaCl、CaCO3,若无色液体A中含有两种溶质,这两种溶质可能是:NaCl、NaOH;
(3)若水为“一定量”,碳酸钠在水中的溶解度较小,无色液体C中有两种溶质,则白色固体D中可能物质组合有:碳酸钠或碳酸钙.
故答案为:(1)CO2;
(2)CaCO3,氢氧化钙、氯化钙或氢氧化钠、氯化钙,NaCl、CaCO3,NaCl、NaOH;
(3)碳酸钠或碳酸钙.
点评 解答本题要从物质的颜色、物质之间相互作用时的实验现象等方面进行分析、判断,从而得出正确的结论;而本题的推断结论的答案不唯一,需要讨论多种可能.

| A. |  点燃酒精灯 | B. |  读取液体体积 | C. |  过滤 | D. | 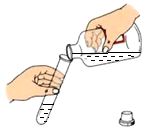 倾倒液体 |
| A. | 用氧气供呼吸 | B. | 用石墨作电极 | ||
| C. | 用水银填充温度计 | D. | 用氦气填充气球 |
| A. | 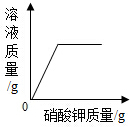 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | |
| B. | 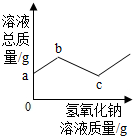 在含有氯化铁的稀盐酸中滴加氢氧化钠溶液 在含有氯化铁的稀盐酸中滴加氢氧化钠溶液 | |
| C. | 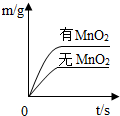 两份质量和浓度都相同的H2O2溶液在有无MnO2的情况下,产生O2的质量与时间t的关系 两份质量和浓度都相同的H2O2溶液在有无MnO2的情况下,产生O2的质量与时间t的关系 | |
| D. | 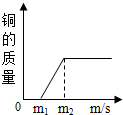 在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉 在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉 |
