题目内容
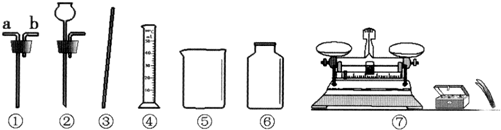
实验室中要配制一定溶质质量分数的氯化钠溶液,请你帮助完成.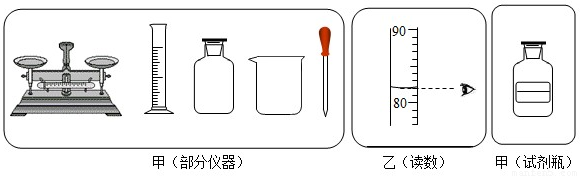
(1)甲图中缺少一种必须用到的玻璃仪器是______(填写名称).
(2)准确称量18g氯化钠,量取蒸馏水的体积如乙图所示,氯化钠完全溶解后所配制的溶液中溶质的质量分数是______(水的密度为1g/cm3).
(3)配制氯化钠溶液的操作过程依次是:氯化钠的称量、水的量取、______、装瓶并贴上标签.请你把丙图中试剂瓶上的标签填写完整.
【答案】分析:(1)根据配制溶液的操作过程确定所需要的仪器,与图进行对比,找出图中所缺仪器;
(2)根据溶质质量分数的计算公式进行解答;
(3)根据配制氯化钠溶液的操作过程依次是:氯化钠的称量、水的量取、溶解、装瓶并贴上标签进行解答.
解答:解:(1)图中缺少玻璃棒,该仪器在溶解操作中用于搅拌;
(2)图示所量取水的体积为82mL,因此所配制溶液的质量分数=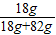 ×100%≈18%;
×100%≈18%;
(3)配制氯化钠溶液的操作过程依次是:氯化钠的称量、水的量取、溶解、装瓶并贴上标签;标签至少要写上溶液名称及溶质质量分数,因此,标签上应写上:18%NaCl溶液.
故答案为:(1)玻璃棒;(2)18%;(3)溶解;18%NaCl溶液.
点评:抓住导致配制溶液时所出现误差的根本原因:溶质量或多或少、溶剂量或多或少,分析操作对溶质、溶剂量所造成的影响,使配制溶液出现误差类问题可以轻松解决.
(2)根据溶质质量分数的计算公式进行解答;
(3)根据配制氯化钠溶液的操作过程依次是:氯化钠的称量、水的量取、溶解、装瓶并贴上标签进行解答.
解答:解:(1)图中缺少玻璃棒,该仪器在溶解操作中用于搅拌;
(2)图示所量取水的体积为82mL,因此所配制溶液的质量分数=
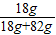 ×100%≈18%;
×100%≈18%;(3)配制氯化钠溶液的操作过程依次是:氯化钠的称量、水的量取、溶解、装瓶并贴上标签;标签至少要写上溶液名称及溶质质量分数,因此,标签上应写上:18%NaCl溶液.
故答案为:(1)玻璃棒;(2)18%;(3)溶解;18%NaCl溶液.
点评:抓住导致配制溶液时所出现误差的根本原因:溶质量或多或少、溶剂量或多或少,分析操作对溶质、溶剂量所造成的影响,使配制溶液出现误差类问题可以轻松解决.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
木炭粉还原氧化铜实验后的混合粉末中含有铜、氧化铜、少量木炭粉,实验室从该混合粉末中回收铜的方案如下:

(1)写出下列反应的化学方程式:反应①:______; 反应②:______.
(2)反应①所用的硫酸的质量分数为24.5%.现要配制40g 24.5%的硫酸,需______g 98%的硫酸和______g水.
(3)在进行“反应①”、“反应②”、“反应③”的操作时,可将反应物加入______中(填仪器名称),然后______ (填操作名称),使反应充分进行.
(4)试剂A可选用______溶液(填一种物质的化学式)
(5)已知某合金粉末除铝外,还含有铁、铜中的一种或两种.某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
【猜想】猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有______(填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
【探究结论】猜想3成立.
【反思】一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式______.

(1)写出下列反应的化学方程式:反应①:______; 反应②:______.
(2)反应①所用的硫酸的质量分数为24.5%.现要配制40g 24.5%的硫酸,需______g 98%的硫酸和______g水.
(3)在进行“反应①”、“反应②”、“反应③”的操作时,可将反应物加入______中(填仪器名称),然后______ (填操作名称),使反应充分进行.
(4)试剂A可选用______溶液(填一种物质的化学式)
(5)已知某合金粉末除铝外,还含有铁、铜中的一种或两种.某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
【猜想】猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有______(填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的______,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有______. |
| ②取步骤①所得滤渣,加过量的______,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有______. |
【反思】一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式______.