题目内容
13.某化学小组同学研究铁丝在氧气中燃烧的反应,进行了如下实验,取一段打磨好的螺旋状铁丝,在下面系一根火线,点燃火柴,待火柴快燃尽时,插入充满氧气且放有少量水的集气瓶中,观察到如下现象,铁丝下端熔成一个小铁球,生成一种黑色固体,做完实验以后小明对该实验有两个问题疑惑不解,分别做了以下探究实验:【问题一】掉落下来的黑色固体中是否仍然含有铁?为了确定该黑色固体的成分,同学们查阅以下资料
①铁粉是黑色或灰黑色粉末,四氧化三铁为黑色固体,具有磁性.
②四氧化三铁和盐酸反应:Fe3O4+8HCl═2FeCl3+FeCl2+4H2O
有同学提出:用磁铁来确定黑色固体的成分,其他同学表示反对,其理由为铁和四氧化三铁都能被磁铁吸引.
经过讨论,同学们设计了以下实验方案,通过实验确定了黑色固体的成分.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量黑色固体于试管中,加入适量盐酸,放置一段时间 | 现象1:液体由无色变为黄色 | 黑色固体中含有四氧化三铁 |
| 现象2:有气泡冒出 | 黑色固体中含有铁 |
查阅资料:①FeO在空气中极易被氧化为Fe2O3.
②Fe2O3绝Fe3O4的分解度和熔点见下表:
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | |
| 熔点/℃ | 1535 |
拓展延伸
(1)有些食品包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色由黑色变为红色,就说明包装盒破损透气,这样售货员就能及时发现并处理;
(2)下列铁的氧化物中,铁元素的质量分数由大到小的顺序是A>C>B(填字母).
A、FeO B、Fe2O3 C、Fe3O4
(3)Fe2O3高温时分解成Fe3O4和一种气体,请写出该反应的方程式6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑.
分析 根据已有的知识进行分析解答,四氧化三铁和铁都能被磁铁吸引,根据四氧化三铁与盐酸反应的生成物、铁与盐酸反应的生成物判断;根据氧化亚铁能被氧化为氧化铁,颜色发生改变解答;根据化学式计算元素的质量分数,根据反应物和生成物以及反应的条件书写反应的化学方程式.
解答 解:【问题一】铁和四氧化三铁都能被磁铁吸引,故不能用磁铁来确定黑色固体的成分,故填:铁和四氧化三铁都能被磁铁吸引.
四氧化三铁能与盐酸反应生成氯化铁,水溶液变黄,铁能与盐酸反应产生气体,会观察到气泡产生,故填:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量黑色固体于试管中,加入适量盐酸,放置一段时间 | 现象1:液体由无色变为黄色 | 黑色固体中含有四氧化三铁 |
| 现象2:有气泡冒出 | 黑色固体中含有铁 |
故答案为:1535---1538;Fe2O3.
拓展延伸
(1)有些食品包装盒的透明盖内放有黑色的FeO粉末,氧化亚铁能被氧气氧化生成氧化铁,颜色由黑色变为红色,故填:由黑色变为红色;
(2)将铁的氧化物的化学式改写,可以变为:A、Fe6O6,B、Fe6O9;C、Fe6O8;故铁元素的质量分数由大到小的顺序是A>C>B;故填:A>C>B;
(3)Fe2O3高温时分解成Fe3O4和氧气,故填:6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑.
点评 解答本题容易出错的地方是铁丝燃烧的温度范围,要知道铁丝燃烧需要达到熔点才能开始燃烧,温度不能超过四氧化三铁的分解温度,否则就得不到四氧化三铁了.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
3.如图是超市里一种盐汽水的营养成分表.
(1)该汽水中能量很低,主要由碳水化合物
(2)该汽水中含人体每天所需的六大营养素有3种.
(2)“钠118毫克”是指元素(填“单质”或“元素”)的质量;100mL汽水中含氯化钠300.1毫克.
(3)小虎同学欲探究该盐汽水的酸碱性,取少量汽水于试管中,滴加紫色石蕊试液,石蕊试液变红色,则该汽水显酸性,经查阅资料该汽水中溶有大量的CO2,要提高100mL水中CO2的溶解量,可加压、降温(写两种方法即可).要证明盐汽水中含CO2,可用_振荡塑料瓶将气体通入澄清石灰水的方法检验CO2的存在.
| 项目 | 每100毫克 | 单位 | 营养素参考值% |
| 能量 | 43 | 千焦 | 1% |
| 蛋白质 | 0 | 克 | 0% |
| 脂肪 | 0 | 克 | 0% |
| 碳水化合物 | 25 | 克 | 1% |
| 钠 | 118 | 毫克 | 6% |
(2)该汽水中含人体每天所需的六大营养素有3种.
(2)“钠118毫克”是指元素(填“单质”或“元素”)的质量;100mL汽水中含氯化钠300.1毫克.
(3)小虎同学欲探究该盐汽水的酸碱性,取少量汽水于试管中,滴加紫色石蕊试液,石蕊试液变红色,则该汽水显酸性,经查阅资料该汽水中溶有大量的CO2,要提高100mL水中CO2的溶解量,可加压、降温(写两种方法即可).要证明盐汽水中含CO2,可用_振荡塑料瓶将气体通入澄清石灰水的方法检验CO2的存在.
4.NaCl、KNO3在不同温度下溶解度的数据如表:
(1)50℃时,硝酸钾的溶解度为85.5g.
(2)在60℃时,100g水中加入120g硝酸钾,充分搅拌后所得溶液质量为210g.
(3)70℃时,100g饱和NaCl溶液冷却到10℃时,溶液的质量<(选填“>”或“<”或“=”)100g.
(4)由表中数据分析可知,硝酸钾和氯化钠在某一温度范围时具有相同的溶解度,则该温度范围是20~30℃.
(5)欲从海水中获得氯化钠晶体,应采取蒸发溶剂的方法.
| 温度℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | |
(2)在60℃时,100g水中加入120g硝酸钾,充分搅拌后所得溶液质量为210g.
(3)70℃时,100g饱和NaCl溶液冷却到10℃时,溶液的质量<(选填“>”或“<”或“=”)100g.
(4)由表中数据分析可知,硝酸钾和氯化钠在某一温度范围时具有相同的溶解度,则该温度范围是20~30℃.
(5)欲从海水中获得氯化钠晶体,应采取蒸发溶剂的方法.
8.同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行研究.
(1)写出上述化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑,反应后溶液中一定有氯化钠.对可能含有的物质进行探究.
(2)确定废液中是否含有盐酸:
①选用如图1所示物质X是酸碱指示剂中的石蕊溶液.
②向废液中加入少量的镁粉,观察到无气泡产生(或无现象或无变化),确定废液中一定没有盐酸.
(3)确定废液中是否含有Na2CO3,可选用pH试纸(或pH计)测出废液的pH=10,确定废液中一定含有Na2CO3.
(4)欲从废液中得到纯净的NaCl,请完成如下实验方案设计.
(5)按如图2方案分离BaCl2和NaCl的固体混合物时,X溶液中溶质是溶质是Na2CO3.

(1)写出上述化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑,反应后溶液中一定有氯化钠.对可能含有的物质进行探究.
(2)确定废液中是否含有盐酸:
①选用如图1所示物质X是酸碱指示剂中的石蕊溶液.
②向废液中加入少量的镁粉,观察到无气泡产生(或无现象或无变化),确定废液中一定没有盐酸.
(3)确定废液中是否含有Na2CO3,可选用pH试纸(或pH计)测出废液的pH=10,确定废液中一定含有Na2CO3.
(4)欲从废液中得到纯净的NaCl,请完成如下实验方案设计.
| 方案 | 加入试剂 | 分离方法 | 方案评价 |
| 一 | 适量Ca(NO3)2 | 过滤、蒸发结晶 | 不可行,理由是引进新杂质(或有NaNO3,生成或引进NO3-) |
| 二 | 稍过量的盐酸(或稀HCl或HCl) | 蒸发结晶 | 可行 |
18.下列基本实验操作正确的是( )
| A. | 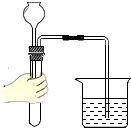 检查气密性 检查气密性 | B. |  闻药品的气味 | C. | 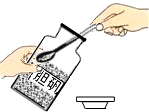 取固体药品 | D. | 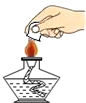 熄灭酒精灯 |
5.下列关于金刚石和石墨的说法正确的是( )
| A. | 都是由碳元素组成的单质 | B. | 他们的物理性质和化学性质都相似 | ||
| C. | 都能导电,做电池电极 | D. | 硬度都很大,能做铅笔芯 |
 如图是元素周期表的一部分,这三种元素均位于第三周期,等质量的三种元素中所含原子个数由多到少的顺序是钠、镁、铝,三种元素原子的最外层电子数目依次为1、2、3.
如图是元素周期表的一部分,这三种元素均位于第三周期,等质量的三种元素中所含原子个数由多到少的顺序是钠、镁、铝,三种元素原子的最外层电子数目依次为1、2、3. 中和〇分别表示两种不同的原子,其中表示化合物的是( )
中和〇分别表示两种不同的原子,其中表示化合物的是( )


