题目内容
某化合物在氧气中完全燃烧后生成二氧化碳和水,已知生成的二氧化碳和水的质量比为22:9,则该化合物的化学式可能是( )
A.C2H2
B.C2H4
C.C2H5OH
D.CH4
【答案】分析:本题可以利用化学方程式来比较得出答案,也可以根据质量守恒定律,化学反应前后元素的质量相等来计算,后者更为简便.
解答:解:根据二氧化碳和水的质量比为22:9,可计算出碳、氢两种元素的质量比为(22×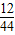 ):(9×
):(9×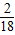 )=6:1,根据质量守恒定律可知碳、氢元素均来自该化合物,所以其中碳氢原子的个数比是
)=6:1,根据质量守恒定律可知碳、氢元素均来自该化合物,所以其中碳氢原子的个数比是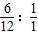 =1:2,观察选项只有B中碳氢原子的个数比是2:1;其它均不符合两者的个数比;
=1:2,观察选项只有B中碳氢原子的个数比是2:1;其它均不符合两者的个数比;
故选B.
点评:本题考查元素质量比的计算,及质量守恒定律的灵活运用,解题的关键是化学反应前后元素的质量相等;
解答:解:根据二氧化碳和水的质量比为22:9,可计算出碳、氢两种元素的质量比为(22×
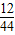 ):(9×
):(9×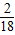 )=6:1,根据质量守恒定律可知碳、氢元素均来自该化合物,所以其中碳氢原子的个数比是
)=6:1,根据质量守恒定律可知碳、氢元素均来自该化合物,所以其中碳氢原子的个数比是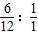 =1:2,观察选项只有B中碳氢原子的个数比是2:1;其它均不符合两者的个数比;
=1:2,观察选项只有B中碳氢原子的个数比是2:1;其它均不符合两者的个数比;故选B.
点评:本题考查元素质量比的计算,及质量守恒定律的灵活运用,解题的关键是化学反应前后元素的质量相等;

练习册系列答案
相关题目