题目内容
16.下列各组物质,在pH=11的溶液中,可能大量存在的是( )| A. | 硫酸钠 氯化钾 | B. | 氯化氢 碳酸钾 | C. | 氯化铜 硝酸钾 | D. | 氯化钠 氯化铵 |
分析 pH为11的水溶液显碱性,水溶液中含有大量的OH-.根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存,据此进行分析判断即可.
解答 解:pH为11的水溶液显碱性,水溶液中含有大量的OH-.
A、硫酸钠、氯化钾在溶液中相互交换成分不能生成沉淀、气体、水,能在碱性溶液中大量共存,故选项正确.
B、氯化氢溶于水,和碱性溶液中的氢氧根离子能结合生成水,氯化氢溶于水与碳酸钾交换成分生成氯化钾、水和二氧化碳,不能大量共存,故选项错误.
C、氯化铜中的铜离子和碱性溶液中的氢氧根离子能结合生成氢氧化铜沉淀,不能大量共存,故选项错误.
D、氯化铵中的铵根离子和碱性溶液中的氢氧根离子能结合生成氨气和水,不能大量共存,故选项错误.
故选:A.
点评 本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水;还要注意在碱性溶液中共存.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.空气中体积分数约为$\frac{1}{5}$的气体是( )
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 稀有气体 |
1.如图四个图象能正确反映对应变化关系的是( )
| A. |  加热一定质量的高锰酸钾 | B. |  将镁片放入硝酸铜溶液中 | ||
| C. |  木炭在密闭的容器内燃烧 | D. |  电解水生成两种气体 |
5.下列物质属于混合物的是( )
| A. | 蒸馏水 | B. | 氧气 | C. | 空气 | D. | 一氧化碳 |

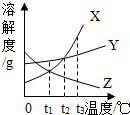 如图表示X、Y、Z三种物质的溶解度曲线,下列说法正确的是C
如图表示X、Y、Z三种物质的溶解度曲线,下列说法正确的是C