题目内容
 碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小朵同学设计了实验,以探究碳酸氢钠的化学性质.
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小朵同学设计了实验,以探究碳酸氢钠的化学性质.【探究实验1】碳酸氢钠溶液的酸碱性
【实验方案】取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞溶液,振荡
现象:溶液变成浅红色.由此得出结论
【探究实验2】能与酸反应
【实验方案】取少量该固体加入试管中,滴加稀盐酸,现象为
【探究实验3】碳酸氢钠的热稳定性
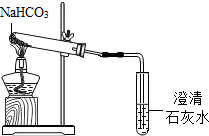
【实验方案】用如图所示装置进行实验
现象:充分加热后,大试管口有水珠出现,管底有白色固体残留,小试管中澄清石灰水变浑浊
结论:碳酸氢钠受热能生成二氧化碳、水和一种白色固体
验证:(1)请你帮小朵设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH(所选试剂不能用酸)
步骤:
(2)试写出碳酸氢钠受热反应的化学方程式
拓展:写出碳酸氢钠在日常生活中的一种用途
考点:盐的化学性质,证明碳酸盐,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:碱性溶液能使酚酞试液变红;
碳酸盐和酸反应生成二氧化碳;
根据反应物和生成物书写化学方程式;
区分碳酸钠和氢氧化钠可用含钙离子的溶液,根据生成沉淀区别.
碳酸钙不溶于水;
根据碳酸氢钠能和酸反应的性质填空.
碳酸盐和酸反应生成二氧化碳;
根据反应物和生成物书写化学方程式;
区分碳酸钠和氢氧化钠可用含钙离子的溶液,根据生成沉淀区别.
碳酸钙不溶于水;
根据碳酸氢钠能和酸反应的性质填空.
解答:解:【探究实验1】因为碱性溶液能使酚酞变红,所以此现象说明碳酸氢钠溶液呈碱性;
【探究实验2】碳酸氢钠和盐酸反应二氧化碳气体,会看到溶液中能产生气泡.反应的化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑;
【探究实验3】(1)碳酸钠能和氢氧化钙反应生成沉淀,而氢氧化钠和氢氧化钙不反应,故取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水,若溶液变浑浊,则白色固体为碳酸钠;
(2)碳酸氢钠受热发生反应的化学方程式:2NaHCO3
Na2CO3+H2O+CO2↑,为分解反应;
碳酸氢钠能和酸反应生成二氧化碳,故可以用作治疗胃酸的药物(或用作发酵粉).
故答案为:【探究实验1】碳酸氢钠溶液呈碱性;
【探究实验2】产生气泡,NaHCO3+HCl═NaCl+H2O+CO2↑;
【探究实验3】(1)取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水;溶液变浑浊;
(2)2NaHCO3
Na2CO3+H2O+CO2↑,分解;
治疗胃酸的药物(或用作发酵粉).
【探究实验2】碳酸氢钠和盐酸反应二氧化碳气体,会看到溶液中能产生气泡.反应的化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑;
【探究实验3】(1)碳酸钠能和氢氧化钙反应生成沉淀,而氢氧化钠和氢氧化钙不反应,故取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水,若溶液变浑浊,则白色固体为碳酸钠;
(2)碳酸氢钠受热发生反应的化学方程式:2NaHCO3
| ||
碳酸氢钠能和酸反应生成二氧化碳,故可以用作治疗胃酸的药物(或用作发酵粉).
故答案为:【探究实验1】碳酸氢钠溶液呈碱性;
【探究实验2】产生气泡,NaHCO3+HCl═NaCl+H2O+CO2↑;
【探究实验3】(1)取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水;溶液变浑浊;
(2)2NaHCO3
| ||
治疗胃酸的药物(或用作发酵粉).
点评:碳酸盐和酸反应放出二氧化碳气体,二氧化碳能使石灰水变浑浊,碳酸盐溶液能和含钙离子的溶液反应生成沉淀.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
下列不属于化学变化的是( )
| A、葡萄酿酒 | B、钢铁生锈 |
| C、酒精燃烧 | D、汽油挥发 |
加热150mL液体需要用到的仪器有( )
| ① | ② | ③ | ④ | ⑤ | ⑥ |
 |
 |
 |
 |
 |
 |
| A、①③④⑥ | B、②③④⑥ |
| C、②③④⑤ | D、①③④⑤ |
地壳中各元素的质量分数由多到少排列正确的是( )
| A、氧、铝、硅、铁 |
| B、硅、氧、铁、铝 |
| C、铁、铝、氧、硅 |
| D、氧、硅、铝、铁 |
2011年3月11日,日本发生了震惊世界的大地震.地震灾害过程中发生的下列变化中与其他三项不同的一种是( )
| A、山体滑坡 | B、房屋倒塌 |
| C、铁轨扭曲 | D、仓库爆炸 |

 某同学对蜡烛(主要成分是石蜡)及其燃烧进行如下探究.请填写下列空格:
某同学对蜡烛(主要成分是石蜡)及其燃烧进行如下探究.请填写下列空格: