题目内容
为了探究影响化学反应速度的因素,某同学设计实验如下:| 实验一 | 实验二 | |
| 实验 过程 |  |  |
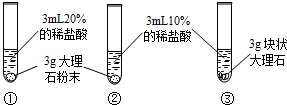
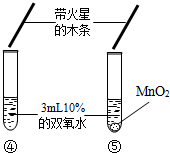
| 实验现象 | 大理石表面冒气泡,试管外壁微热.试管①、②、③中产生气泡快慢的顺序为:①>②>③. | 试管④中无明显现象,⑤中可观察到大量的气泡,两只试管上方的木条均未复燃. |
| 分析与 结论 | (1)大理石与稀盐酸反应的化学方程式为______; (2)对比实验①②可知,______,化学反应的速度越快;对比实验______(填实验序号)可知,反应物的接触面积越大,化学反应的速度越快. | (1)对比实验④⑤可知,影响化学反应速度的因素还有______; (2)试管⑤中产生了大量氧气,但是木条却未复燃,可能的一种原因是 ______. |
【答案】分析:解答此类题的关键是找准对比实验中的变量,对比题意中的设计方案,结合图形给予的信息,可以分析得出:大理石粉末与浓度比较大的盐酸反应快,块状大理石与稀盐酸反应慢,过氧化氢在有催化剂的条件下反应快.
解答:解:实验一(1)大理石与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)对比实验①②,所用盐酸的浓度不同,可得出反应物的浓度越大,化学反应的速度越快;对比实验 ②③,反应物的接触面不同,可知,反应物的接触面积越大,化学反应的速度越快.
实验二(1)对比实验④⑤,不同点是有无催化剂,根据现象可知,影响化学反应速度的因素还有催化剂;
(2)从燃烧的条件分析,试管⑤中产生了大量氧气,但是木条却未复燃,可能的一种原因是氧气中混有水蒸气,使木条达不到燃烧的温度.
故答案为:
实验一
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)反应物的浓度越大;②③.
实验二
(1)催化剂;
(2)氧气中混有水蒸气.
点评:此题主要是对于反应物的种类和状态影响了反应的速度作出了探究,并培养了学生对于科学实验的实事求是的精神.
解答:解:实验一(1)大理石与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)对比实验①②,所用盐酸的浓度不同,可得出反应物的浓度越大,化学反应的速度越快;对比实验 ②③,反应物的接触面不同,可知,反应物的接触面积越大,化学反应的速度越快.
实验二(1)对比实验④⑤,不同点是有无催化剂,根据现象可知,影响化学反应速度的因素还有催化剂;
(2)从燃烧的条件分析,试管⑤中产生了大量氧气,但是木条却未复燃,可能的一种原因是氧气中混有水蒸气,使木条达不到燃烧的温度.
故答案为:
实验一
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)反应物的浓度越大;②③.
实验二
(1)催化剂;
(2)氧气中混有水蒸气.
点评:此题主要是对于反应物的种类和状态影响了反应的速度作出了探究,并培养了学生对于科学实验的实事求是的精神.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
以下是某研究小组 探究影响化学反应速率部分因素的相关实验数据。
探究影响化学反应速率部分因素的相关实验数据。
| 实验 序号 | H2O2溶 液浓 度/% | H2O2溶液 体积/mL |
| MnO2的 用量/g | 收集氧 气的体 积/mL | 反应所需 的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 2 | 49.21 | |
| ④ | 30 | 5 | 55 | 2 | 10.76 |
(1)通过 实验①和②对比可知,化学反应速率与________有关;从实验__________和__________对比可知,化学反应速率与温度的关系是______________________。
实验①和②对比可知,化学反应速率与________有关;从实验__________和__________对比可知,化学反应速率与温度的关系是______________________。
(2)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的概率有关。试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是____________________________。
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产 生氧气的总重量________(选填“减小”“不变”或“增大”)。
生氧气的总重量________(选填“减小”“不变”或“增大”)。
某同学为了探究影响过氧化氢和二氧化锰制取氧气的反应速率的影响因素,通过实验得到下表的数据:请认真分析表中数据,回答下列问题:
(1)通过实验①和②对比可知,化学反应速率与______有关;
(2)从实验③和④对比可知,化学反应速率与温度的关系是______;
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量______(选填“减小”或“不变”或“增大”).
| 实验 序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/ml | 温度/℃ | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所需的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | --------------- | 2 | 49.21 |
| ④ | 30 | 5 | 55 | --------------- | 2 | 10.76 |
(2)从实验③和④对比可知,化学反应速率与温度的关系是______;
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量______(选填“减小”或“不变”或“增大”).