题目内容
(2011?浦东新区一模)为了探究影响化学反应速度的因素,某同学设计实验如下:
| 实验一 | 实验二 | |
| 实验 过程 |
 |
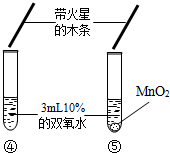 |
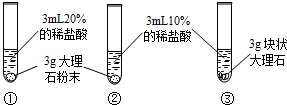
| 实验现象 | 大理石表面冒气泡,试管外壁微热.试管①、②、③中产生气泡快慢的顺序为:①>②>③. | 试管④中无明显现象,⑤中可观察到大量的气泡,两只试管上方的木条均未复燃. |
| 分析与 结论 |
(1)大理石与稀盐酸反应的化学方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ ;(2)对比实验①②可知, 反应物的浓度越大 反应物的浓度越大 ,化学反应的速度越快;对比实验②③ ②③ (填实验序号)可知,反应物的接触面积越大,化学反应的速度越快. |
(1)对比实验④⑤可知,影响化学反应速度的因素还有 催化剂 催化剂 ;(2)试管⑤中产生了大量氧气,但是木条却未复燃,可能的一种原因是 氧气中混有水蒸气 氧气中混有水蒸气 . |
分析:解答此类题的关键是找准对比实验中的变量,对比题意中的设计方案,结合图形给予的信息,可以分析得出:大理石粉末与浓度比较大的盐酸反应快,块状大理石与稀盐酸反应慢,过氧化氢在有催化剂的条件下反应快.
解答:解:实验一(1)大理石与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)对比实验①②,所用盐酸的浓度不同,可得出反应物的浓度越大,化学反应的速度越快;对比实验 ②③,反应物的接触面不同,可知,反应物的接触面积越大,化学反应的速度越快.
实验二(1)对比实验④⑤,不同点是有无催化剂,根据现象可知,影响化学反应速度的因素还有催化剂;
(2)从燃烧的条件分析,试管⑤中产生了大量氧气,但是木条却未复燃,可能的一种原因是氧气中混有水蒸气,使木条达不到燃烧的温度.
故答案为:
实验一
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)反应物的浓度越大;②③.
实验二
(1)催化剂;
(2)氧气中混有水蒸气.
(2)对比实验①②,所用盐酸的浓度不同,可得出反应物的浓度越大,化学反应的速度越快;对比实验 ②③,反应物的接触面不同,可知,反应物的接触面积越大,化学反应的速度越快.
实验二(1)对比实验④⑤,不同点是有无催化剂,根据现象可知,影响化学反应速度的因素还有催化剂;
(2)从燃烧的条件分析,试管⑤中产生了大量氧气,但是木条却未复燃,可能的一种原因是氧气中混有水蒸气,使木条达不到燃烧的温度.
故答案为:
实验一
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)反应物的浓度越大;②③.
实验二
(1)催化剂;
(2)氧气中混有水蒸气.
点评:此题主要是对于反应物的种类和状态影响了反应的速度作出了探究,并培养了学生对于科学实验的实事求是的精神.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
 +4Cu
+4Cu ”内对应产物的化学式为
”内对应产物的化学式为