题目内容
9.下列描述的是某些实验部分现象,其中正确的是( )| A. | 将少量生铁放入足量的稀硫酸中,有少量固体没有溶解 | |
| B. | 电解水时,正、负电极上产生的气体体积比为2:1 | |
| C. | 镁条在空气中燃烧时也会产生一些白色烟雾 | |
| D. | 一定温度时,向饱和氯化钠溶液中加入氯化钠固体,看到固体逐渐溶解 |
分析 A、根据生铁是铁和碳组成的合金,铁会与酸反应生成氢气,碳不会与酸反应进行分析;
B、根据电解水时,正、负电极上产生的气体是氧气和氢气,体积比为1:2进行分析;
C、根据镁和氧气在点燃的条件下生成氧化镁进行分析;
D、根据饱和溶液的定义进行分析.
解答 解:A、生铁是铁和碳组成的合金,铁会与酸反应生成氢气,碳不会与酸反应,所以将少量生铁放入足量的稀硫酸中,有少量固体没有溶解,故A正确;
B、电解水时,正、负电极上产生的气体是氧气和氢气,体积比为1:2,故B错误;
C、镁和氧气在点燃的条件下生成氧化镁,所以镁条在空气中燃烧时也会产生一些白烟,故C错误;
D、饱和溶液就是在一定温度下,不能再溶解某种溶质的溶液,所以一定温度时,向饱和氯化钠溶液中加入氯化钠固体,固体不能溶解,故D错误.
故选:A.
点评 本题主要考查了化学中常见的一些基础知识,难度不大,需要在平时的学习中加强记忆即可完成.

练习册系列答案
相关题目
4.下列物质的俗称和化学式相一致的是( )
| A. | 纯碱--NaOH | B. | 生石灰--CaO | C. | 水银--Ag | D. | 石灰水--Ca(OH)2 |
1.为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动.
【探究活动一】检验硬化的氢氧化钙样品是否完全变质
(1)检验氢氧化钙样品是否完全变质,进行如下实验,请将实验步骤和现象补充完整:
【探究活动二】测定样品中含有的变质固体(以下用R表示)的质量分数:
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数.实验装置(气密性良好)如图1所示.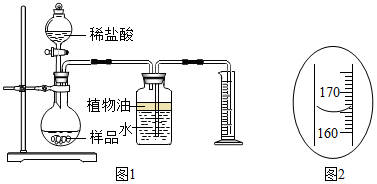
(2)实验中量筒的作用是收集排出的水,从而确定反应生成二氧化碳的体积.
(3)实验结束后,量筒内进入水的体积如图2所示.已知在该实验条件下,生成气体的密度为2克/升,通过计算,样品中R的质量分数为25%.
(4)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因:稀盐酸进入烧瓶导致计算的二氧化碳体积偏大(写一个).
【探究活动一】检验硬化的氢氧化钙样品是否完全变质
(1)检验氢氧化钙样品是否完全变质,进行如下实验,请将实验步骤和现象补充完整:
| 实验步骤和现象 | 实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水 充分混合后静置,滴加酚酞试液,酚酞试液变红色 | 该样品还含有氢氧化钙 |
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数.实验装置(气密性良好)如图1所示.

(2)实验中量筒的作用是收集排出的水,从而确定反应生成二氧化碳的体积.
(3)实验结束后,量筒内进入水的体积如图2所示.已知在该实验条件下,生成气体的密度为2克/升,通过计算,样品中R的质量分数为25%.
(4)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因:稀盐酸进入烧瓶导致计算的二氧化碳体积偏大(写一个).
18.维生素是人体必需的营养物质,维生素D2的化学式为C28H44O.下列说法正确的是( )
| A. | 维生素D2属于有机化合物 | B. | 维生素D2中含有73个原子 | ||
| C. | 维生素D2的相对分子质量是396g | D. | 维生素D2中氢元素的质量分数最大 |



