题目内容
在一密闭容器中有X、Y、Z、W四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示.下列说法中正确的是
( )
| 物质 | X | Y | Z | W |
| 反应前质量/g | 8 | 10 | 1 | 21 |
| 反应后质量/g | 0 | 21 | 待测 | 9 |
A.反应后Z的质量为9g
B.反应中Y与W发生改变的质量比为1:1
C.反应生成Y的质量为11g
D.Z在该反应中作催化剂
【考点】质量守恒定律及其应用.
【专题】压轴实验题;化学用语和质量守恒定律.
【分析】根据质量守恒定律:参加化学反应的各物质质量总和等于反应后生成的各物质质量总和.反应后质量增加了说明是生成物,质量减少了是反应物,质量不变是催化剂.
【解答】解:X质量反应后减少,是反应物且参加反应的质量为:8g﹣0=8g,Y的质量反应后增加了,是生成物,且生成了21g﹣10g=11g,W质量反应后减少属于反应物,参加反应的质量为:21g﹣9g=12g,由参加化学反应的各物质质量总和等于反应后生成的各物质质量总和,可知Z属于生成物,且生成的质量为:8g+12g﹣11g=9g,所以Z的待测质量为:9g+1g=10g.
故选C.
【点评】做这类题目的关键是反应后质量和反应前进行比较,质量增加了说明是生成物,质量减少了是反应物,质量不变可能是催化剂.

 快乐5加2金卷系列答案
快乐5加2金卷系列答案铝镁合金因密度小、强度高、刚性好等特点,在人类生活中应用广泛.某兴趣小组的同学对编号为①、②的两种铝镁合金样品进行了如下实验.
已知:镁能与酸反应,但不能与碱溶液反应;铝既能与酸反应,又能与氢氧化钠等碱溶液反应,化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,NaAlO2溶液与二氧化碳反应能产生氢氧化铝沉淀,后者经过滤、洗涤、灼烧后生成相应氧化物.
(1)取质量为m的样品①和过量的氢氧化钠溶液反应,然后过滤;再向滤液中通入过量的二氧化碳气体,将所得沉淀过滤、洗涤、烘干、灼烧,所得固体的质量仍为m.求样品①中铝的质量分数.
(2)取不同质量的样品②分别和30 g相同浓度的盐酸反应,所取合金质量与产生气体体积(气体的密度为0.089 3 g/L)如表所示:
| 实验序号 | a | b | c |
| 合金质量/mg | 510 | 765 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
求:合金中铝镁的质量比.
 性质: ;
性质: ;
 2Fe+3CO2,
2Fe+3CO2,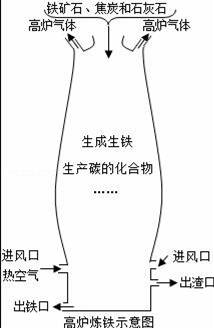


 B.
B.

 D.
D.



 CaO+CO2↑
CaO+CO2↑
 海水晒盐 B.
海水晒盐 B.
 风力发电C.
风力发电C.
 铁矿石炼铁 D.
铁矿石炼铁 D.
 太阳能取暖
太阳能取暖