��Ŀ����
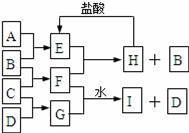
��þ�Ͻ����ܶ�С��ǿ�ȸߡ����Ժõ��ص㣬������������Ӧ�ù㷺��ij��ȤС���ͬѧ�Ա��Ϊ�١��ڵ�������þ�Ͻ���Ʒ����������ʵ�飮 ��
��֪��þ�����ᷴӦ�������������Һ��Ӧ�����������ᷴӦ���������������Ƶȼ���Һ��Ӧ����ѧ����ʽΪ��2Al+2NaOH+2H2O�T2NaAlO2+3H2����NaAlO2��Һ�������̼��Ӧ�ܲ��������������������߾����ˡ�ϴ�ӡ����պ�������Ӧ�����
��1��ȡ����Ϊm����Ʒ�ٺ���������������Һ��Ӧ��Ȼ����ˣ�������Һ��ͨ������Ķ�����̼���壬�����ó������ˡ�ϴ�ӡ���ɡ����գ����ù����������Ϊm������Ʒ������������������������
��2��ȡ��ͬ��������Ʒ�ڷֱ��30 g��ͬŨ�ȵ����ᷴӦ����ȡ�Ͻ�������������������������ܶ�Ϊ0.089 3 g/L�������ʾ��
| ʵ����� | a | b | c |
| �Ͻ�����/mg | 510 | 765 | 918 |
| �������/mL | 560 | 672 | 672 |
�Ͻ�����þ�������ȣ�
�����㡿���ݻ�ѧ��Ӧ����ʽ�ļ��㣮
��ר�⡿�йػ�ѧ����ʽ�ļ��㣮
����������1�����ݷ����Ļ�ѧ��Ӧ��2Al+2NaOH+2H2O�T2NaAlO2+3H2����NaAlO2+CO2+2H2O=NaHCO3+Al��OH��3����2Al��OH��3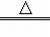
 Al2O3+3H2O�����õ��Ĺ��������������������䣬˵������������Ԫ�ص�������������þԪ�ص�����������
Al2O3+3H2O�����õ��Ĺ��������������������䣬˵������������Ԫ�ص�������������þԪ�ص�����������
��2�����ݱ����ṩ�������ж����ᷴӦ�������ٽ��м��㣮
����𡿽⣺��1��2Al+2NaOH+2H2O�T2NaAlO2+3H2����NaAlO2+CO2+2H2O=NaHCO3+Al��OH��3����2Al��OH��3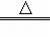
 Al2O3+3H2O�����õ��Ĺ��������������������䣬˵������������Ԫ�ص�������������þԪ�ص���������������Ԫ�ص�����������������������Ԫ�ص�����������
Al2O3+3H2O�����õ��Ĺ��������������������䣬˵������������Ԫ�ص�������������þԪ�ص���������������Ԫ�ص�����������������������Ԫ�ص�����������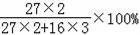
 ��52.9%��
��52.9%��
��2���ݱ�����Կ�������һ�εĺϽ�ȫ���μӷ�Ӧ�����ɵ�����������Ϊ��0.56L��0.0893g/L��0.05g
��þ������Ϊx�����ɵ�����������Ϊa������������Ϊ0.51g��x�����ɵ�����������Ϊ0.05g��a
Mg+2HCl�TMgCl2+H2��
24 2
x a
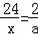

2Al+6HCl�T2AlCl3+3H2��
54 6
0.51g��x 0.05g��a
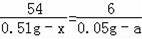

���x=0.24g��
����������Ϊ0.51g��0.24g=0.27g
������þ��������Ϊ��0.27g��0.24g=9��8
�𣺺Ͻ�����þ��������Ϊ9��8��
��������������Ҫ����ѧ�����û�ѧ����ʽ���м�����ƶϵ�����������ʱҪע��淶�Ժ�ȷ�ԣ�

��һ�ܱ���������X��Y��Z��W�������ʣ���һ�������³�ַ�Ӧ����÷�Ӧǰ������ʵ��������±���ʾ������˵������ȷ����
��������
| ���� | X | Y | Z | W |
| ��Ӧǰ����/g | 8 | 10 | 1 | 21 |
| ��Ӧ������/g | 0 | 21 | ���� | 9 |
A����Ӧ��Z������Ϊ9g
B����Ӧ��Y��W�����ı��������Ϊ1��1
C����Ӧ����Y������Ϊ11g
D��Z�ڸ÷�Ӧ��������
�������и����������õ����ַ�������ȷ���ǣ�������
| ѡ�� | ��Ҫ���ֵ����� | ����һ | ������ |
| A | �Ȼ�����Ȼ��� | �ֱ�����ʯ�һ����ĥ | �۲���ɫ |
| B | ʳ�κʹ��� | ��ʳ�� | �ܽ⣬�μ��Ȼ�����Һ |
| C | ���������������� | �ܽ⣬�μӷ�̪��Һ | ��ζ�� |
| D | ��ë����� | ��ȼ������ζ | �۲�ɫ�� |
A��A B��B C��C D��D