籾朕坪否
和双麗嵎嶄鑓圷殆嵎楚蛍方喇互欺詰電双屎鳩議頁
- A.FeO﹅Fe2O3﹅Fe3O4﹅FeS
- B.Fe2O3﹅FeO﹅Fe3O4﹅FeS
- C.Fe3O4﹅Fe2O3﹅FeO﹅FeS
- D.FeO﹅Fe3O4﹅Fe2O3﹅FeS
D
蛍裂⦿↙1⇄圭隈匯⦿功象蝶圷殆議嵎楚蛍方= 〜100%栖蛍艶柴麻箔竃宸膨嶽麗嵎嶄鑓圷殆議嵎楚蛍方曳熟寄弌軸辛◉
〜100%栖蛍艶柴麻箔竃宸膨嶽麗嵎嶄鑓圷殆議嵎楚蛍方曳熟寄弌軸辛◉
↙2⇄圭隈屈⦿S圷殆議屢斤圻徨嵎楚頁32⇧方峙屢輝噐2倖O圻徨議屢斤圻徨嵎楚◉絞辛參繍S心撹頁曾倖剳圻徨◉壅鉱賀膨嶽麗嵎議晒僥塀蛍艶脅算麻撹1倖鑓圻徨斤哘叱倖剳圻徨◉夸剳圻徨方埆寄議鑓圷殆議嵎楚蛍方祥埆弌⤴
盾基⦿↙1⇄Fe0嶄鑓圷殆議嵎楚蛍方葎⦿ 100%=77.8%◉
100%=77.8%◉
Fe2O3嶄鑓圷殆議嵎楚蛍方葎⦿ 〜100%=70%◉
〜100%=70%◉
Fe3O4嶄鑓圷殆議嵎楚蛍方葎⦿ 100%=72.4%◉
100%=72.4%◉
FeS嶄鑓圷殆議嵎楚蛍方葎⦿ 100%=63.6%⤴
100%=63.6%⤴
夸鑓圷殆嵎楚蛍方喇互欺詰電双⦿FeO﹅Fe3O4﹅Fe2O3﹅FeS⤴
↙2⇄咀葎S圷殆議屢斤圻徨嵎楚頁32⇧方峙屢輝噐2倖O圻徨議屢斤圻徨嵎楚◉
絞辛參繍S心撹頁曾倖剳圻徨◉
鉱賀膨嶽麗嵎議晒僥塀辛岑⦿FeO嶄匯倖鑓圻徨斤哘1倖剳圻徨⇧Fe3O4嶄匯倖鑓圻徨斤哘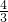 倖剳圻徨⇧Fe2O3嶄匯倖鑓圻徨斤哘
倖剳圻徨⇧Fe2O3嶄匯倖鑓圻徨斤哘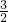 倖剳圻徨⇧FeS嶄匯倖鑓圻徨斤哘2倖剳圻徨◉
倖剳圻徨⇧FeS嶄匯倖鑓圻徨斤哘2倖剳圻徨◉
夸剳圻徨方埆寄議鑓圷殆議嵎楚蛍方祥埆弌◉
絞鑓圷殆嵎楚蛍方喇互欺詰電双⦿FeO﹅Fe3O4﹅Fe2O3﹅FeS⤴
絞僉D⤴
泣得⦿緩籾勣箔曳熟圷殆嵎楚蛍方議互詰⤴塰喘巷塀幟匯柴麻匆嬬宥狛柴麻潤惚曳熟⇧徽湊訓末⤴酔堀盾籾議圭隈頁延塀箔揖隈⤴委巷塀延撹葎叟噐蛍裂議侘塀⇧匯違音心廬晒朔議屢揖何蛍⇧遇肇蛍裂曳熟餓呟議何蛍⇧軸辛誼竃潤胎⤴
蛍裂⦿↙1⇄圭隈匯⦿功象蝶圷殆議嵎楚蛍方=
 〜100%栖蛍艶柴麻箔竃宸膨嶽麗嵎嶄鑓圷殆議嵎楚蛍方曳熟寄弌軸辛◉
〜100%栖蛍艶柴麻箔竃宸膨嶽麗嵎嶄鑓圷殆議嵎楚蛍方曳熟寄弌軸辛◉↙2⇄圭隈屈⦿S圷殆議屢斤圻徨嵎楚頁32⇧方峙屢輝噐2倖O圻徨議屢斤圻徨嵎楚◉絞辛參繍S心撹頁曾倖剳圻徨◉壅鉱賀膨嶽麗嵎議晒僥塀蛍艶脅算麻撹1倖鑓圻徨斤哘叱倖剳圻徨◉夸剳圻徨方埆寄議鑓圷殆議嵎楚蛍方祥埆弌⤴
盾基⦿↙1⇄Fe0嶄鑓圷殆議嵎楚蛍方葎⦿
 100%=77.8%◉
100%=77.8%◉Fe2O3嶄鑓圷殆議嵎楚蛍方葎⦿
 〜100%=70%◉
〜100%=70%◉Fe3O4嶄鑓圷殆議嵎楚蛍方葎⦿
 100%=72.4%◉
100%=72.4%◉FeS嶄鑓圷殆議嵎楚蛍方葎⦿
 100%=63.6%⤴
100%=63.6%⤴夸鑓圷殆嵎楚蛍方喇互欺詰電双⦿FeO﹅Fe3O4﹅Fe2O3﹅FeS⤴
↙2⇄咀葎S圷殆議屢斤圻徨嵎楚頁32⇧方峙屢輝噐2倖O圻徨議屢斤圻徨嵎楚◉
絞辛參繍S心撹頁曾倖剳圻徨◉
鉱賀膨嶽麗嵎議晒僥塀辛岑⦿FeO嶄匯倖鑓圻徨斤哘1倖剳圻徨⇧Fe3O4嶄匯倖鑓圻徨斤哘
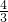 倖剳圻徨⇧Fe2O3嶄匯倖鑓圻徨斤哘
倖剳圻徨⇧Fe2O3嶄匯倖鑓圻徨斤哘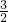 倖剳圻徨⇧FeS嶄匯倖鑓圻徨斤哘2倖剳圻徨◉
倖剳圻徨⇧FeS嶄匯倖鑓圻徨斤哘2倖剳圻徨◉夸剳圻徨方埆寄議鑓圷殆議嵎楚蛍方祥埆弌◉
絞鑓圷殆嵎楚蛍方喇互欺詰電双⦿FeO﹅Fe3O4﹅Fe2O3﹅FeS⤴
絞僉D⤴
泣得⦿緩籾勣箔曳熟圷殆嵎楚蛍方議互詰⤴塰喘巷塀幟匯柴麻匆嬬宥狛柴麻潤惚曳熟⇧徽湊訓末⤴酔堀盾籾議圭隈頁延塀箔揖隈⤴委巷塀延撹葎叟噐蛍裂議侘塀⇧匯違音心廬晒朔議屢揖何蛍⇧遇肇蛍裂曳熟餓呟議何蛍⇧軸辛誼竃潤胎⤴

膳楼過狼双基宛
 畠嬬霞陣豚挑弌彜圷狼双基宛
畠嬬霞陣豚挑弌彜圷狼双基宛
屢購籾朕
和双麗嵎嶄鑓圷殆嵎楚蛍方喇互欺詰電双屎鳩議頁↙ ⇄
| A、FeO﹅Fe2O3﹅Fe3O4﹅FeS | B、Fe2O3﹅FeO﹅Fe3O4﹅FeS | C、Fe3O4﹅Fe2O3﹅FeO﹅FeS | D、FeO﹅Fe3O4﹅Fe2O3﹅FeS |

