题目内容
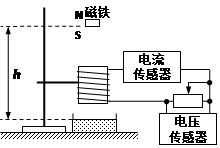
某同学利用如图装置研究磁铁下落过程中的重力势能与电能之间的相互转化。内阻r=40Ω的螺线管固定在铁架台上,线圈与电流传感器、电压传感器和滑动变阻器连接。滑动变阻器最大阻值40Ω,初始时滑片位于正中间20Ω的位置。打开传感器,将质量为m的磁铁置于螺线管正上方静止释放,磁铁上表面为N极。穿过螺线管后掉落到海绵垫上并静止(磁铁下落中受到的电磁阻力远小于磁铁重力,不发生转动),释放点到海绵垫高度差为h。计算机屏幕上显示出如图的UI-t曲线。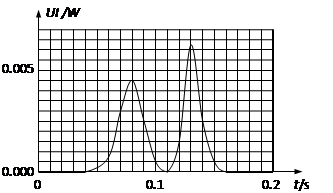
(1)磁铁穿过螺线管过程中,产生第一峰值时线圈中的感应电动势约 V。
(2)图像中UI出现前后两个峰值,对比实验过程发现,这两个峰值是在磁铁刚进入螺线管内部和刚从内部出来时产生的,对这一现象相关说法正确的是 ( )
| A.线圈中的磁通量变化率经历先增大后减小再增大再减小的过程 |
| B.如果滑片从中间向左移动时,坐标系中的两个峰值一定都会减小 |
| C.磁铁在穿过线圈过程中加速度始终小于重力加速度g |
| D.如果仅略减小h,两个峰值都会减小 |
(1)由图像可以直接读出功率的峰值为0.0045W,电压传感器测量的是滑动变阻器两端电压,电阻为20欧姆,由
 ,滑动变阻器两端电压峰值为0.3V,再由串联分压可知电感线圈产生的电动势峰值为0.9V(2)由感应电动势公式
,滑动变阻器两端电压峰值为0.3V,再由串联分压可知电感线圈产生的电动势峰值为0.9V(2)由感应电动势公式 可知A对;如果滑片从中间向左移动时,不会改变螺线管产生的感应电动势,峰值不变,B错;由楞次定律可知磁铁在穿过线圈过程中始终受到竖直向上的磁场力的作用,加速度始终小于重力加速度,C对;减小高度h,穿过螺线管时的速度减小,坐标系中的两个峰值一定都会减小,D对;(3)由能量守恒6.3´10-4J—6.9´10-4J
可知A对;如果滑片从中间向左移动时,不会改变螺线管产生的感应电动势,峰值不变,B错;由楞次定律可知磁铁在穿过线圈过程中始终受到竖直向上的磁场力的作用,加速度始终小于重力加速度,C对;减小高度h,穿过螺线管时的速度减小,坐标系中的两个峰值一定都会减小,D对;(3)由能量守恒6.3´10-4J—6.9´10-4J 
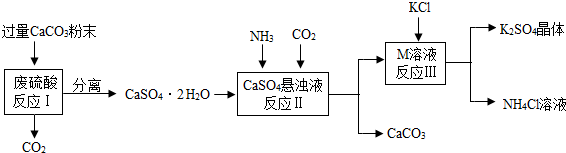
某实验小组利用废硫酸液制备K2SO4并研究CaSO4•2H2O加热分解的产物.
(一)K2SO4的制备

(1)将CaCO3研成粉末的目的是 .
(2)上述流程中可循环使用的物质有CO2和 (填写化学式).
(3)反应Ⅲ中相关物质的溶解度如下表.你认为反应Ⅲ在常温下能实现的原因是 .
|
物质 |
KCl |
K2SO4 |
NH4Cl |
M |
|
溶解度/g(25℃) |
34.0 |
11.1 |
37.2 |
19.5 |
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是 ;为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入 (选填序号,下同),振荡、静置,再向上层清液中滴加 ,观察现象即可判断.
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液
(二)研究CaSO4•2H2O加热分解的产物.
(5)分离所得的CaSO4•2H2O含有CaCO3,可用盐酸除去,该的化学反应方程式 .
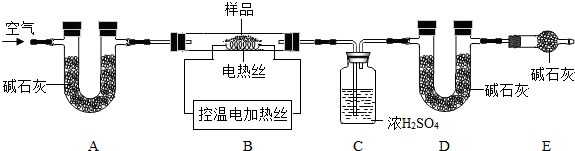
(6)为了测定CaSO4•2H2O和CaCO3的质量比x:y,实验小组利用如图所示的装置(夹持仪器省略)进行实验.

①实验前首先要 ,再装入样品.装置A的作用是 .
②已知CaSO4•2H2O在160℃生成CaSO4,1350℃时CaSO4开始分解;CaCO3在900℃时分解完全.现控制B装置温度900℃进行实验并采集了如下数据:
a.反应前玻璃管与样品的质量m1g b.反应后玻璃管中固体的质量为m2g
c.装置C实验后增重m3g d.装置D实验后增重m4g
某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将 (填“偏大”、“偏小”或“无影响”).你认为还可选用上述的 (选填序号)两个数据组合也可求出x:y的值.
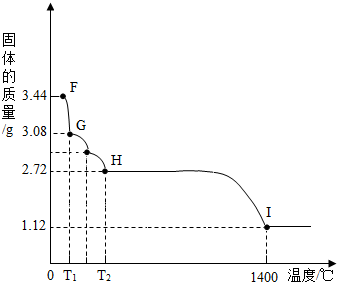
(7)CaSO4•2H2O受热会逐步失去结晶水.取纯净CaSO4•2H2O固体3.44g,放在(5)的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示.①G点固体的化学式是 .

②将T2~1400℃温度段加热固体所产生的气体通入酸性KMnO4溶液中,溶液褪色,则H~I段发生反应的化学方程式为 .
某校化学小组对热水壶底部水垢的主要成分进行了如下探究,请完成以下活动并回答相关问题.
【查阅资料】天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见下表(20℃):
| 阴离子 阳离子 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
【提出问题】水垢的主要成分中是否含有Ca(OH)2和MgCO3呢?
【实验方案1】确定水垢中是否含Ca(OH)
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液. | 没有白色沉淀产生 | 水垢中______. |
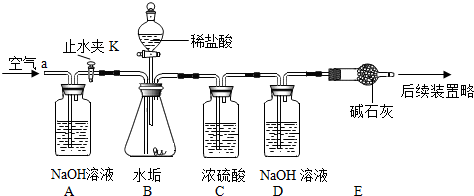
利用如图所示的实验装置,完成实验2探究.其主要实验步骤如下:
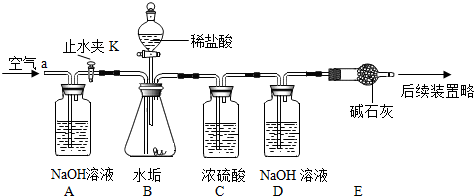
精确称量D、E装置总质量为600.0g,按上图组装后,将9.8g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为604.4g(碱石灰主要成分为CaO和NaOH,不考虑稀盐酸的挥发性以及装置内空气、外界空气对实验的影响).
【实验讨论】
(1)加入药品前应______,反应结束后打开止水夹K,缓缓鼓入空气的目的是______.
(2)任写一个装置B中生成气体的化学反应方程式:______.
(3)装置 B中生成CO2的质量为______g.通过计算说明该水垢中______(填序号)含MgCO3.
A.一定 B.一定不 C.可能 D.无法确定
【实验方案3】定量探究水垢中氢氧化镁的质量分数
另取质量为9.8g的水垢试样,加入7.3%稀盐酸与之恰好完全反应,测得消耗稀盐酸110g.结合以上数据和实验结论,计算水垢样品中氢氧化镁的质量分数(写出完整的计算过程,计算结果保留一位小数).
(一)K2SO4的制备

(1)将CaCO3研成粉末的目的是 .
(2)上述流程中可循环使用的物质有CO2和 (填写化学式).
(3)反应Ⅲ中相关物质的溶解度如下表.你认为反应Ⅲ在常温下能实现的原因是 .
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液
(二)研究CaSO4?2H2O加热分解的产物.
(5)分离所得的CaSO4?2H2O含有CaCO3,可用盐酸除去,该的化学反应方程式 .
(6)为了测定CaSO4?2H2O和CaCO3的质量比x:y,实验小组利用如图所示的装置(夹持仪器省略)进行实验.

①实验前首先要 ,再装入样品.装置A的作用是 .
②已知CaSO4?2H2O在160℃生成CaSO4,1350℃时CaSO4开始分解;CaCO3在900℃时分解完全.现控制B装置温度900℃进行实验并采集了如下数据:
a.反应前玻璃管与样品的质量m1g b.反应后玻璃管中固体的质量为m2g
c.装置C实验后增重m3g d.装置D实验后增重m4g
某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将 (填“偏大”、“偏小”或“无影响”).你认为还可选用上述的 (选填序号)两个数据组合也可求出x:y的值.
(7)CaSO4?2H2O受热会逐步失去结晶水.取纯净CaSO4?2H2O固体3.44g,放在(5)的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示.①G点固体的化学式是 .

②将T2~1400℃温度段加热固体所产生的气体通入酸性KMnO4溶液中,溶液褪色,则H~I段发生反应的化学方程式为 .