题目内容
10.要配制50g10%NaCl溶液,试回答下列问题:(1)需要NaCl5g,水45毫升
(2)实验所需仪器药匙、托盘天平、量筒、玻璃棒、烧杯、胶头滴管
(3)量筒是选用100mL的还是50mL?50mL.原因是选择量筒时,所选量筒的量程要超过液体的体积且接近性原则,以减小实验的误差.
(4)某同学用天平称量NaCl时,误将药品放在右盘中.此时,他称得NaCl的质量为5.1g,(1g以下用游码)则该同学称得的NaCl的实际质量为4.9g.
分析 (1)根据溶质质量分数公式可以计算出所需氯化钠的质量和水的体积解答;
(2)根据实验药品的取用所需的仪器、溶液配制所需的实验仪器作答;
(3)根据选取量筒的原则进行量筒的选择;
(4)根据天平的使用方法是左物右码,左盘的质量等于右盘的质量加游码的质量,即药品质量=砝码质量+游码质量,如果位置放反,根据左盘的质量=右盘的质量+游码的质量,列等式进行计算.
解答 解:
(1)配制50g 10%的氯化钠溶液时,需要氯化钠的质量为50g×10%=5g,则需水的足量是50g-5g=45g,水的密度是1g/cm3,则体积为45mL;
(2)用到的仪器有:药匙、托盘天平、量筒、玻璃棒、烧杯、胶头滴管;
(3)选择量筒时,所选量筒的量程要超过液体的体积且接近性原则,以减小实验的误差,需水的体积为45mL,则量取水时需要用到50mL的量筒;
(4)由左盘的质量=右盘的质量+游码的质量可知:砝码质量=药品质量+游码的质量,所以药品质量=砝码质量-游码质量,即:药品的质量=5.0g-0.1g=4.9g.
答案:
(1)5;45;
(2)药匙、托盘天平、量筒、玻璃棒、烧杯、胶头滴管;
(3)50mL;选择量筒时,所选量筒的量程要超过液体的体积且接近性原则,以减小实验的误差;
(4)4.9.
点评 本题考查的是溶液的配制,完成此题,可以依据已有的知识进行回答,所以要求同学们在平时的学习中要加强基础知识的储备.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
15.“对人吸入的空气与呼出的气体有什么不同”的探究,请你根据所学的知识,完成下列实验报告.
| 探究目的 | 实验操作 | 实验现象 | 得出结论 |
| 比较空气与呼出气体中含二氧化碳气体的多少 | 取一瓶空气,一瓶呼出的气体,各滴入澄清石灰水,振荡 | ||
| 空气中氧气的含量比呼出气体中的多 | |||
| 向一块干燥玻璃瓶呼气,另取一块干燥玻璃瓶放在空气中 |

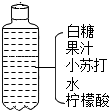 根据图中自制汽水的配料回答问题.
根据图中自制汽水的配料回答问题.