题目内容
19.A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去):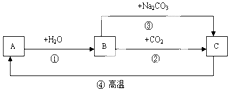
(1)A物质的化学式是CaO,B物质的俗称是熟石灰,
(2)举出B物质在农业生产中的一种用途:改良酸性土壤.
(3)反应③的化学方程式为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,该反应的基本反应类型是复分解反应.
分析 由于A、B、C均是含钙化合物,所以在初中应该在氧化钙、碳酸钙、氢氧化钙之中.由于C能高温分解,所以C为碳酸钙;A是高温煅烧产物,为氧化钙;而氧化钙和水反应能够得到氢氧化钙(B);氢氧化钙与二氧化碳和碳酸钠反应都能得到碳酸钙,据此分析.
解答 解:由于A、B、C均是含钙化合物,所以在初中应该在氧化钙、碳酸钙、氢氧化钙之中.由于C能高温分解,所以C为碳酸钙.A是高温煅烧产物,为氧化钙.而氧化钙和水反应能够得到氢氧化钙(B).氢氧化钙与二氧化碳和碳酸钠反应都能得到碳酸钙.即A:氧化钙;B、氢氧化钙;C、碳酸钙.
(1)根据分析,A物质为氧化钙,在氧化钙中钙元素为+2价的,而氧元素为-2价的,根据在化合物中化合价代数和为零可得其化学式是CaO;B物质为氢氧化钙,其俗称是熟石灰(或消石灰).
(2)根据分析,B为氢氧化钙,碱性,所以可以用来改良酸性土壤,同时本身具有一定的腐蚀性,所以可能用来杀菌消毒.
(3)反应③是氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,对应的方程式为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,由于是两种化合物相互交换成分,生成新的两种化合物,属于基本反应类型的复分解反应.
故答案为:
(1)CaO; 熟石灰(或消石灰).(2)改良酸性土壤(或者杀菌消毒).
(3)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;复分解反应.
点评 本题属于框图式推断题,在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.

练习册系列答案
相关题目
10.下列实验方案中,合理的是( )
| A. | 分离木炭粉和氧化铜:将混合物在空气中充分灼烧 | |
| B. | 验证质量守恒定律:比较镁条燃烧前后固体的质量 | |
| C. | 除去铜粉中的铁粉:向混合物中加入足量的稀盐酸,充分反应后,过滤、洗涤、烘干 | |
| D. | 鉴别空气和二氧化碳:将带火星的木条分别伸入两瓶气体中 |
7.运载“神州十号”飞船的火箭使用偏二甲肼(C2H8N2)作燃料.下列说法不正确的是( )
| A. | 是一种化合物 | B. | 由碳、氢、氮三种元素组成 | ||
| C. | 所含碳元素的质量分数为40% | D. | 碳、氢、氮元素质量比2:8:2 |
4.硅的元素符号为Si,单晶硅是制作电子集成电路的基础材料.用化学方法可制得高纯硅,有关化学反应方程式为:①SiO2+2C═Si(粗硅)+2CO
②Si+3HCl═SiHCl3+H2
③Si+2Cl2═SiCl4
④SiCl4+2H2$\frac{\underline{\;\;△\;\;}}{\;}$Si+4HCl
上述反应③反应类型属于( )
②Si+3HCl═SiHCl3+H2
③Si+2Cl2═SiCl4
④SiCl4+2H2$\frac{\underline{\;\;△\;\;}}{\;}$Si+4HCl
上述反应③反应类型属于( )
| A. | 复分解反应 | B. | 分解反应 | C. | 置换反应 | D. | 化合反应 |
9.小雄通过实验得到下列数据,其中你认为正确的是( )
| A. | 用托盘天平称取了6.8gNaCl | |
| B. | 用pH试纸测得某溶液酸碱度为7.5 | |
| C. | 用量筒量取了15.67mL水 | |
| D. | 常温下,M的溶解度为36g,可配得该温度下36%的M溶液 |
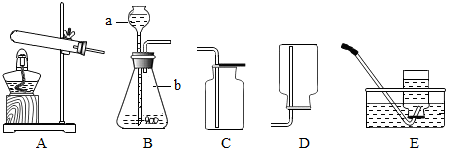
 有一包白色固体可能含碳酸钠、硫酸钠、氯化钾、硝酸钡中的一种或几种.某化学兴趣小组为探究其成分进行了以下实验:
有一包白色固体可能含碳酸钠、硫酸钠、氯化钾、硝酸钡中的一种或几种.某化学兴趣小组为探究其成分进行了以下实验: