题目内容
15.金属钛(Ti)的合金具有耐高温、耐腐蚀、强度高等性能,钛合金广泛用于航空、航天工业及化学工业.工业上以钛铁矿(主要成分FeTiO3,钛酸亚铁)为主要原料冶炼金属钛,同时得到重要的化工原料甲醇(CH3OH).生产的工艺流程图如下(部分产物略去):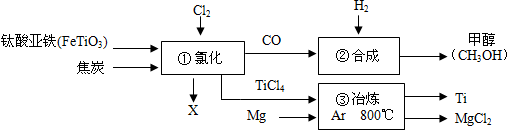
(1)该流程图中涉及到的物质属于有机物的是甲醇.
(2)钛酸亚铁(FeTiO3)中钛元素的化合价为+4.
(3)①中反应为:2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2X+2TiCl4+6CO,则X的化学式为FeCl3.
(4)③所属的基本反应类型为置换反应.
(5)②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1.
分析 (1)根据有机物的定义进行分析;
(2)根据化合价代数和为零进行分析;
(3)根据质量守恒定律可知,在化学反应前后原子个数不变进行分析;
(4)根据反应③是四氯化钛和镁在高温的条件下生成氯化镁和钛进行分析;
(5)根据一氧化碳和氢气全部转化为甲醇,结合化学方程式为进行解答.
解答 解:(1)在物质的组成中含有碳元素的化合物叫有机物,但是一氧化碳、二氧化碳、碳酸钙等具有无机物的性质,属于无机物,所以涉及到的物质属于有机物的是甲醇;
(2)在FeTiO3(钛酸亚铁)中,氧显-2价,铁显+2价,所以钛元素的化合价是+4价;
(3)根据质量守恒定律可知,在化学反应前后原子个数不变,所以X是FeCl3;
(4)反应③是四氯化钛和镁在高温的条件下生成氯化镁和钛,单质和化合物反应生成单质和化合物,属于置换反应;
(5)一氧化碳和氢气合成乙醇,所以CO+2H2=CH3OH,为使原料全部转化为甲醇,理论上CO和H2投料的质量比为28:4=7:1.
故答案为:(1)甲醇;
(2)+4;
(3)FeCl3;
(4)反置换反应;
(5)7:1.
点评 在解此类题时,首先分析题中所给的反应流程,然后结合学过的知识和题中的问题进行解答.

练习册系列答案
 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
6.化学知识在生活中有广泛的应用,下列说法错误的是( )
| A. | 血红蛋白中含有铁元素,缺铁会引起人体贫血 | |
| B. | 回收废弃的塑料可以减少“白色污染” | |
| C. | 肥皂水可以区分硬水和软水 | |
| D. | 室内放一盆水能防止一氧化碳中毒 |
3.人类的发展离不开化学的发展.从远古时代火的使用,到现代各领域都和化学有着千丝万缕的联系.下列变化中不属于化学范畴的是( )
| A. | 景德瓷器的烧制 | B. | 神十宇航员所穿衣服的制作 | ||
| C. | 次超声波的运用 | D. | 安徽宣纸的生产 |
10.下列物质放在水中,能形成溶液的是( )
| A. | 面粉 | B. | 花生油 | C. | 白糖 | D. | 牛奶 |
1.下列说法正确的是( )
| A. | 能生成盐和水的反应一定酸碱中和反应 | |
| B. | 元素的化学性质与原子核外的最外层上的电子数目有密切的关系 | |
| C. | 阴离子得到电子会变成原子 | |
| D. | 由同种元素组成的物质一定是单质 |


