题目内容
12.4.80g金属镁和一定量硫酸锌溶液,充分反应剩余固体质量为8.90g,再将剩余固体加入到足量的硫酸亚铁溶液中,能得金属的质量是( )| A. | 5.6g | B. | 11.2g | C. | 9.6g | D. | 16.8g |
分析 根据镁和硫酸锌反应置换出的锌、剩余的镁都会与硫酸亚铁反应生成铁,依据元素守恒可知,直接用镁和硫酸亚铁反应列出关系式进行计算.
解答 解:设得到金属的质量为x
Mg-----FeSO4----Fe
24 56
4.8g x
$\frac{24}{4.8g}$=$\frac{56}{x}$
x=11.2g
故选:B.
点评 本题主要考查了金属活动性顺序的应用,依据元素守恒的计算,注意认真分析反应原理即可正确解答.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
20.研究和学习化学,有许多方法.下列方法中所举例不正确的是( )
| 选项 | 方法 | 示例 |
| A | 分类法 | 根据组成物质的元素种类,将纯净物分为单质和化合物 |
| B | 类比法 | 根据金属铝能与稀盐酸反应,推测金属铜也能与稀盐酸反应 |
| C | 归纳法 | 根据氢氧化钠、氢氧化钙等物质的化学性质,归纳出碱的通性 |
| D | 实验法 | 用磷做“测定空气中氧气含量”的实验 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
7.如图所示的实验操作不正确的是( )
| A. |  铁丝在氧气中燃烧 | B. |  读取液体的体积 | ||
| C. | 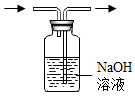 除去CO中的CO2 | D. |  加热液体 |
4.化学实验是科学探究的重要学习方式,下列实验操作正确的是( )
| A. | 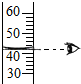 量取液体体积 | B. | 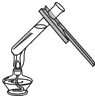 给试管内液体加热 | ||
| C. |  铁丝在氧气中燃烧 | D. | 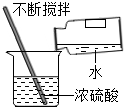 稀释浓硫酸 |