题目内容
7.如图所示,某Vc含片的包装.试求:
(1)Vc分子中碳、氢、氧原子个数比3:4:3;
(2)Vc中C、H、O元素的质量比9:1:12;
(3)维生素 C中氧元素的质量分数54.5%;
(4)若每日服用 2片含片,即可满足每日摄入 500mg维生素的需要.则含片中Vc的含量为12.5%.
分析 (1)根据每个Vc分子的构成进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(4)根据题意,每片Vc含片的质量为2g;若每日服用 2片含片,即可满足每日摄入500mg维生素的需要,据此进行分析解答.
解答 解:(1)1个Vc分子是由6个碳原子、8个氢原子和6个氧原子构成的,则Vc分子中碳、氢、氧三种原子的个数比为6:8:6=3:4:3.
(2)Vc中碳、氢和氧三种元素质量比为(12×6):(1×8):(16×6)=9:1:12.
(3)维生素 C中氧元素的质量分数为$\frac{16×6}{12×6+1×8+16×6}$×100%≈54.5%.
(4)根据题意,每片Vc含片的质量为2g;若每日服用 2片含片,即可满足每日摄入500mg维生素的需要,则每片中含250mg(0.25g)维生素,则含片中Vc的含量为$\frac{0.25g}{2g}$×100%=12.5%.
故答案为:(1)3:4:3;(2)9:1:12;(3)54.5%;(4)12.5%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
12.4.80g金属镁和一定量硫酸锌溶液,充分反应剩余固体质量为8.90g,再将剩余固体加入到足量的硫酸亚铁溶液中,能得金属的质量是( )
| A. | 5.6g | B. | 11.2g | C. | 9.6g | D. | 16.8g |
9.下列描述中表达的是物质化学性质的是( )
| A. | 常温下氢氧化铁是一种红褐色不溶于水的固体 | |
| B. | 石墨具有优良的导电性 | |
| C. | 一氧化碳气体可使人中毒 | |
| D. | 水蒸发产生水蒸气 |
12.化学实验现象是学习化学的重要环节,以下实验现象叙述正确的是( )
| A. | 生锈铁钉加入到稀硫酸中,反应结束后,溶液显浅绿色 | |
| B. | 硫粉在氧气中燃烧,产生蓝光 | |
| C. | 打开浓盐酸的瓶塞,瓶口会出现白雾 | |
| D. | 木炭放入氧气瓶中,燃烧生成使石灰水变浑浊的二氧化碳气体 |
 儿童缺锌会引起食欲不振、发育不良,如图为某种补锌口服液说明书的一部分,请回答:
儿童缺锌会引起食欲不振、发育不良,如图为某种补锌口服液说明书的一部分,请回答: 表示氮原子,下图为气体转换的微观过程,请你根据图示回答下列问题
表示氮原子,下图为气体转换的微观过程,请你根据图示回答下列问题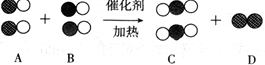
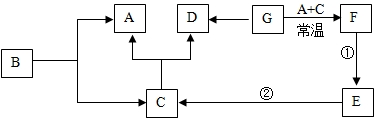 A、B、C、D、E、F、G都是初中化学已学过的常见物质,已知F为红色粉末.它们之间的关系如图所示(图中“→”表示物质间存在转化关系,部分产物及反应条件未标出).
A、B、C、D、E、F、G都是初中化学已学过的常见物质,已知F为红色粉末.它们之间的关系如图所示(图中“→”表示物质间存在转化关系,部分产物及反应条件未标出).