题目内容
18.甲同学设计了如图实验装置探究一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验.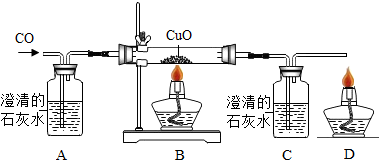
(1)写出加热条件下CO与氧化铜反应的化学方程式:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
该反应中一氧化碳使氧化铜失去氧变成了铜,我们说CO具有还原性.
(2)实验过程中,在图末端的导管口放一盏燃着的酒精灯(灯焰处于导管口),这样做的目的是防止一氧化碳污染空气
(3)CO和CO2的化学性质不同.从微观的角度分析CO和CO2化学性质不同的原因是分子的构成不同
(4)对该实验的分析正确的是(选填编号)ad
a.实验结束时应先熄灭B处酒精灯
b.装置C增加的质量与B中固体减少的质量相等
c.反应开始后通2.8g一氧化碳理论上可生成铜6.35g
d..反应后继续通一氧化碳目的是防止铜被氧化.
分析 (1)根据B中一氧化碳与氧化铜反应生成铜和二氧化碳,进行分析解答.
(2)根据一氧化碳的毒性进行分析解答.
(3)根据CO和CO2的分子构成分析回答;
(4)a.根据一氧化碳还原氧化铜的注意事项进行分析判断.
b.根据C中增加的质量与B中固体减小的质量进行分析判断.
c.根据反应停止后还要继续通入一氧化碳分析
d、根据生成的铜在加热条件下能与氧气反应生成氧化铜,进行分析判断.
解答 解:(1)B中一氧化碳与氧化铜反应生成铜和二氧化碳,反应的化学方程式是:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,该反应中一氧化碳使氧化铜失去氧变成了铜,我们说CO具有还原性.
(2)实验过程中,B中生成的二氧化碳进入C中与氢氧化钙反应生成了碳酸钙沉淀和水,所以,C中的现象是澄清的石灰水变浑浊,由于尾气中含有一氧化碳,一氧化碳能污染空气.所以D处点燃的目的是防止一氧化碳污染空气.
(3)CO和CO2的化学性质不同.从微观的角度分析CO和CO2化学性质不同的原因是分子的构成不同.
(4)a、实验结束时应先熄灭B处酒精灯,故选项说法正确.
b.C中增加的质量是二氧化碳的质量,B中固体减小的质量是氧元素的质量,故质量不相等,故选项说法错误.
C.该反应停止后还要继续通入一氧化碳,所以反应开始后通入2.8g一氧化碳,生成的铜不是2.8g,故选项说法错误;
d、由于生成的铜在加热条件下能与氧气反应生成氧化铜,反应结束后继续通入一氧化碳的目的是防止铜被氧化,故选项说法正确.
故答案为:(1)CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,还原;(2)防止一氧化碳污染空气;(3)分子的构成不同;(4)ad.
点评 本题难度不大,掌握一氧化碳还原氧化铜的反应原理、二氧化碳的化学性质、注意事项等是正确解答本题的关键.

 科学实验活动册系列答案
科学实验活动册系列答案| A. | H2SO4 | B. | O2 | C. | KClO3 | D. | CO2 |
| A. | CH4和NH3 | B. | Ca2+与Cl- | C. | CO2与HCl | D. | OH-与NH-2 |
| A. | 2H2O═O2↑+2H2↑ | B. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2 | D. | KMnO4═K2MnO4+MnO2+O2↑ |
 用如图实验探究分子的性质,试管中固定一张滤纸条,每隔相同距离滴一滴酚酞溶液,将装有适量浓氨水的小药瓶敞口固定在橡皮塞上,一段时间后能观察到的现象是(1)滴有酚酞试液的点由下往上依次变红.
用如图实验探究分子的性质,试管中固定一张滤纸条,每隔相同距离滴一滴酚酞溶液,将装有适量浓氨水的小药瓶敞口固定在橡皮塞上,一段时间后能观察到的现象是(1)滴有酚酞试液的点由下往上依次变红.
