题目内容
3.海水晒盐工业流程中,得到的粗盐常含有MgCl2、CaCl2等杂质,工业提纯粗盐的流程如图所示: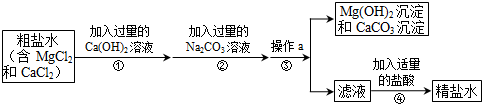
(1)操作a中需要用到玻璃棒,玻璃棒的作用是引流;
(2)步骤①中加入过量Ca(OH)2溶液的目的为完全除去氯化镁;
(3)写出步骤②中发生反应的一个化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(4)操作a后的滤液所含的溶质除了NaCl、Na2CO3外还有NaOH(填化学式)
分析 (1)根据操作a可以将不溶性固体从溶液中分离,所以操作a是过滤,玻璃棒在过滤操作中的作用是引流进行分析;
(2)根据氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙进行分析;
(3)根据碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠与过量的氢氧化钙反应生成碳酸钙沉淀和氢氧化钠进行分析;
(4)根据氢氧化钙和碳酸钠反应会生成碳酸钙沉淀和氢氧化钠进行分析.
解答 解:(1)操作a可以将不溶性固体从溶液中分离,所以操作a是过滤,玻璃棒在过滤操作中的作用是引流;
(2)氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,所以步骤①中加入过量Ca(OH)2溶液的目的为:完全除去氯化镁;
(3)碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠与过量的氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(4)氢氧化钙和碳酸钠反应会生成碳酸钙沉淀和氢氧化钠,所以操作a后的滤液所含的溶质除了NaCl、Na2CO3外还有NaOH.
故答案为:(1)引流;
(2)完全除去氯化镁;
(3)Na2CO3+CaCl2=CaCO3↓+2NaCl;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(4)NaOH.
点评 盐提纯是经常考查的内容,其中要涉及到化学方程式的书写、过滤操作、杂质的除去等内容,需要同学们对此内容了然于心.

练习册系列答案
相关题目
13.夏天防雷电,远离金属.这是因为金属具有( )
| A. | 导热性 | B. | 导电性 | C. | 光泽 | D. | 延展性 |
14.目前电工汽车被称为绿色环保汽车,锂电池是电动汽车的主要动力.新型磷酸亚铁锂(LiFePOX)电池将成为绿色能源的新宠,已知Li、Fe、P的化合价分别为+1、+2、+5,则X的值为( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
18.逻辑推理是化学学习常用的思维方法,下列推理不正确的是( )
| A. | 碱的溶液呈碱性,呈碱性的溶液不一定是碱溶液 | |
| B. | 中和反应生成盐和水,生成盐和水的不一定是中和反应 | |
| C. | 氧化物中一定含氧元素,含氧元素的化合物一定是氧化物 | |
| D. | 单质中只含有一种元素,则只含有一种元素的纯净物一定是单质 |
15.图中所示的四个图象分别表示四个过程,其中正确的是( )
| A. | 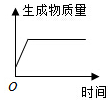 红磷在盛有氧气的密闭容器内燃烧 | B. | 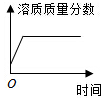 饱和食盐水恒温蒸发 | ||
| C. | 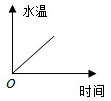 一标准大气压下0℃的冰吸热融化 | D. |  电灯通电后发光 |
17.下列说法正确的是( )
| A. | 汽油去除油污的原理是乳化 | |
| B. | 铜、铁、锌均是人体必需的微量元素 | |
| C. | 铁、生铁、钢均属于合金 | |
| D. | 经常用钢丝球擦拭铝锅,使其保持光亮 |