题目内容
3.金属是人类生活中的常用材料.(1)为了全民的健康,我国推广使用铁强化酱油,这里的“铁”指的是元素(填“单质”、“元素”或“原子”);
(2)人体缺铁会造成B(填字母序号),青少年缺钙会造成C(填字母序号).
A、骨质疏松 B、贫血 C、佝偻病 D、坏血病
(3)要验证锌、铁、铜的活动性顺序,他选择了打磨过的铁丝、硫酸铜溶液,你认为他还需要的溶液是硫酸锌溶液.还可选用物质是锌片、铁片、铜片和稀硫酸.
要探究铁和锌与稀硫酸反应的快慢,需要控制不变(相同)的量ABD(填序号).
A、两种金属的形状 B、硫酸的质量分数 C、反应容器的大小 D、温度
(4)该同学查阅资料得知,铜锈的主要成分是碱式碳酸铜【Cu2(OH)2CO3,相对分子质量为222】,他以铜锈为原料设计并完成如下实验(杂质不与稀硫酸反应,且不含铜元素.图中部分物质略去).

①无色气体A是二氧化碳,固体D的成分是铁、铜;
②已知铜锈样品的质量分数是10g,固体F的质量是3.2g,则铜锈中含Cu2(OH)2CO3的质量分数是55.5%(结果精确至0.1%).
分析 (1)根据物质的组成常用元素来描述分析判断;
(2)根据元素与人体健康之间的关系分析回答;
(3)要验证三种金属的活动性顺序,常采用“三取中”的方法分析回答;
(4)根据实验现象可以判断物质的名称,通过计算可以确定Cu2(OH)2CO3的质量分数.
解答 解:(1)物质的组成常用元素来描述,为了全民的健康,我国推广使用铁强化酱油,这里的“铁”指的是元素;
(2)人体缺铁会造成贫血,青少年缺钙会造成佝偻病;
(3)要验证三种金属的活动性顺序,常采用“三取中”的方法,所以,要验证锌、铁、铜的活动性顺序,他选择了打磨过的铁丝、硫酸铜溶液,你认为他还需要的溶液是硫酸锌溶液.还可选用物质是锌片、铁片、铜片和稀硫酸.要探究铁和锌与稀硫酸反应的快慢,根据控制变量法可知,需要控制不变(相同)的量是两种金属的形状、硫酸的质量分数和温度.
(4)①碱式碳酸铜和稀硫酸反应能生成硫酸铜、水和二氧化碳,无色气体是二氧化碳;向固体D中加入过量稀硫酸时,产生无色气体,是氢气,是由稀硫酸和铁反应生成的,说明铁粉过量,溶液C中所含的溶质是硫酸亚铁;固体D中含有生成的铜和过量的铁粉.
②:设Cu2(OH)2CO3的质量分数为X,
固体F是铜,即生成的铜的质量是3.2g,
10g×X×$\frac{128}{222}$×100%=3.2g,
X=55.5%.
故答为:(1)元素;(2)B,C;(3)硫酸锌,ABD;(4)①二氧化碳,铜、铁粉;②55.5%.
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,有助于提高观察实验、进行实验的能力.

练习册系列答案
相关题目
15.下列物质中,前者是混合物,后者属于碱的是( )
| A. | 碘酒 纯碱 | B. | 冰水混合物 熟石灰 | ||
| C. | 酒精 氨水 | D. | 稀硫酸 烧碱 |
8.下列实验操作中,正确的是( )
| A. |  读取液体体积 | B. |  稀释浓硫酸 | C. |  给液体加热 | D. |  测溶液pH |
15.下列四个实验中,“操作-图象-结论”对应关系正确的是( )
| A | B | C | D | |
| 操作 | 分别向相同质量的镁粉、铁粉、锌粉中加入等浓度稀硫酸 | 一定温度下,向氢氧化钙溶液中加入氧化钙固体 | 向变质的氢氧化钠溶液中滴加稀盐酸 | 将一定量硫酸铜溶液中加入铁粉 |
| 图象 |  | 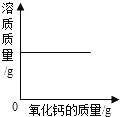 | 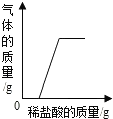 |  |
| 结论 | 三种金属与硫酸反应的剧烈程度:Mg>Zn>Fe | 该氢氧化钙溶液已经饱和 | 氢氧化钠溶液已经全部变质 | 铁与硫酸铜发生了化学反应 |
| A. | A | B. | B | C. | C | D. | D |
13.为防止骨质疏松,应补充的元素是( )
| A. | 铁 | B. | 锌 | C. | 钙 | D. | 碳 |
 生活中处处有化学,请用所学的化学知识填空.
生活中处处有化学,请用所学的化学知识填空. 根据如图回答下列问题.
根据如图回答下列问题.