题目内容
15.下列四个实验中,“操作-图象-结论”对应关系正确的是( )| A | B | C | D | |
| 操作 | 分别向相同质量的镁粉、铁粉、锌粉中加入等浓度稀硫酸 | 一定温度下,向氢氧化钙溶液中加入氧化钙固体 | 向变质的氢氧化钠溶液中滴加稀盐酸 | 将一定量硫酸铜溶液中加入铁粉 |
| 图象 |  | 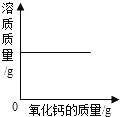 | 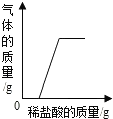 |  |
| 结论 | 三种金属与硫酸反应的剧烈程度:Mg>Zn>Fe | 该氢氧化钙溶液已经饱和 | 氢氧化钠溶液已经全部变质 | 铁与硫酸铜发生了化学反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据横坐标是稀硫酸,消耗硫酸质量相等时,生成氢气质量相等考虑;
B、根据氧化钙与水反应生成氢氧化钙考虑;
C、加入盐酸开始没有气泡产生,是因为盐酸先与氢氧化钠反应;
D、根据铁与硫酸铜反应溶液质量的变化考虑.
解答 解:A、横坐标是稀硫酸,消耗硫酸质量相等时,生成氢气质量相等,如图所示的图横坐标应该改成时间就可以了,故A错;
B、由于氧化钙与水反应生成氢氧化钙,所以氢氧化钙溶液中的溶剂质量减少,因为溶剂减少,溶解不了的溶质会结晶析出,所以溶质质量也减少,故B错;
C、加入盐酸后,开始没有气泡产生,说明盐酸先与氢氧化钠反应,进而产生气体是盐酸和碳酸钠反应生成二氧化碳,所以氢氧化钠部分变质而非完全变质,故C错;
D、铁与硫酸铜反应生成铜和硫酸亚铁,由于进入溶液的铁的质量小于制取出来的铜的质量,所以溶液质量减少,反应完毕,溶液质量不变了,故D正确.
故选D.
点评 解答本题关键是要熟悉对照实验的设计思路,知道氧化钙与水反应生成氢氧化钙,在酸与碱反应、酸与盐反应时,酸与碱反应优先..

练习册系列答案
相关题目
8.下列关于初中化学常见物质的性质或用途的说法正确的是( )
| A. | 木炭有吸附性,可用降低水的硬度 | |
| B. | 熟石灰有吸水性,可用作气体干燥剂 | |
| C. | 火碱常用于治疗胃酸过多 | |
| D. | 硫酸常用于汽车铅蓄电池 |
10.下列认识不正确的是( )
| A. | 在书写具有保存价值的档案时,最好使用碳素笔 | |
| B. | 二氧化碳是一种能产生温室效应的气体 | |
| C. | 生铁和钢主要成分都是铁,但它们的含碳量不同 | |
| D. | 铝制品很耐腐蚀,是因为铝的化学性质很稳定 |
7.某同学在化学记录本上有如下记录,你认为不正确的是( )
| A. | 配平化学方程式的依据是质量守恒定律 | |
| B. | 从元素周期表中可以查出元素的相对原子质量 | |
| C. | 用澄清石灰水可鉴别空气、氧气、二氧化碳、氮气四种气体 | |
| D. | 化学反应发生时不一定能观察到明显的现象 |
5.质量守恒定律是自然界的普遍规律,请用相关知识完成下列问题.
(1)某化合物在氧气中完全燃烧生成二氧化碳和水,推测该化合物中一定含有的元素是C、H;
(2)卫星运载火箭的动力由高氯酸铵(NH4ClO4)发生反应提供,化学方程式为:2NH4ClO4$\frac{\underline{\;高温\;}}{\;}$N${\;}_{{2}_{\;}}$↑+Cl2↑+2O2↑+4X.则X的化学式为H2O;
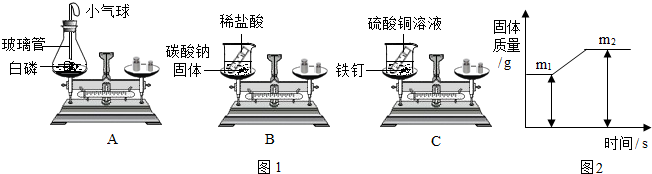
(3)用图1所示的三个实验验证质量守恒定律,其中实验前后天平不能保持平衡的是B(填序号),理由是B是在敞口的容器中反应且生成了气体;
(4)从微观角度分析化学反应有助于我们理解质量守恒定律,在一密闭容器内有4种物质A、B、C、D,它们在一定条件下发生化学反应,经过一段时间后停止反应.A、B、C、D的微观示意图和反应前后物质的质量如下表所示.
①反应中A、B、C、D四种物质属于生成物的是BC;
②表中x的值是108;
③从微观角度分析,化学反应中质量守恒的原因是原子的种类、原子的数目和原子的质量都没有发生改变.
(5)镁带在一密闭容器中与氧气完全燃烧后生成氧化镁,其固体质量变化可用图2表示,则质量差(M2-M1)表示的意义是参加反应的氧气的质量.

(1)某化合物在氧气中完全燃烧生成二氧化碳和水,推测该化合物中一定含有的元素是C、H;
(2)卫星运载火箭的动力由高氯酸铵(NH4ClO4)发生反应提供,化学方程式为:2NH4ClO4$\frac{\underline{\;高温\;}}{\;}$N${\;}_{{2}_{\;}}$↑+Cl2↑+2O2↑+4X.则X的化学式为H2O;
(3)用图1所示的三个实验验证质量守恒定律,其中实验前后天平不能保持平衡的是B(填序号),理由是B是在敞口的容器中反应且生成了气体;
(4)从微观角度分析化学反应有助于我们理解质量守恒定律,在一密闭容器内有4种物质A、B、C、D,它们在一定条件下发生化学反应,经过一段时间后停止反应.A、B、C、D的微观示意图和反应前后物质的质量如下表所示.
| 物质 | A | B | C | D |  |
| 微观示意图 | 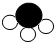 |  |  |  | |
| 反应前质量/g | 100 | 20 | y | x | |
| 反应后质量/g | 32 | 140 | 108 | 0 |
②表中x的值是108;
③从微观角度分析,化学反应中质量守恒的原因是原子的种类、原子的数目和原子的质量都没有发生改变.
(5)镁带在一密闭容器中与氧气完全燃烧后生成氧化镁,其固体质量变化可用图2表示,则质量差(M2-M1)表示的意义是参加反应的氧气的质量.


