题目内容
15.某兴趣小组对Zn(锌)、Ni(镍》、Cu(铜)的金属活动性顺序展开了探究.查阅了部分含镍化合物的溶解性如表,且得知镍能与酸反应.现做实验如下:(1)同温下,取大小、厚度相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
| 阴离子 镍离子 | OH- | NO3- | SO42- | Cl- |
| Ni2+ | 不 | 溶 | 溶 | 溶 |
| 金属 | Ni | Zn | Cu |
| 与盐酸反应的现象 | 气体产生缓慢 金属逐渐溶解 | 气体产生激烈金属迅速溶解 | 无气泡产生 |
(1)上述实验步骤有欠缺,请设计完善实验前,应用砂纸打磨三种金属,除去表面的氧化膜.
(2)将表格中实验现象填写完整.
(3)得出Zn,Ni(镍)、Cu的金属活动性顺序是Zn>Ni>Cu,写出镍与盐酸反应的化学方程式Ni+2HCl=NiCl2+H2↑.
(4)请选择另一类别的一种试剂设计实验.也同样达到一次验证上述假设的正确与否.写出你选择试剂的化学式Zn、NiSO4、Cu.
分析 根据金属的性质进行分析,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,可以从反应生成氢气的速度判断金属的活动性,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,设计实验证明金属的活动性强弱,可以依据金属活动性顺序的意义及金属的性质进行.
解答 解:(1)实验前,应用砂纸打磨三种金属,除去表面的氧化膜;
(2)铜排在氢的后面,不能与酸反应,所以无明显现象;
(3)通过金属与酸反应的剧烈程度可得出锌比镍活泼,而铜排在氢的后面,所以最不活泼;得出Zn,Ni(镍)、Cu的金属活动性顺序是Zn>Ni>Cu;
镍+2价,镍与酸的反应可类比其它活泼金属;镍与盐酸反应的化学方程式为:Ni+2HCl=NiCl2+H2↑;
(4)镍比铜活泼所以可以和硫酸铜溶液反应;把锌和铜放入硫酸镍溶液中锌的表面有黑色固体出现,铜没有明显变化,可得出结论.
答案是:
(1)实验前,应用砂纸打磨三种金属,除去表面的氧化膜;
(2)
| 金属 | Ni | Zn | Cu |
| 与盐酸反应的现象 | 气体产生缓慢 金属逐渐溶解 | 气体产生激烈金属迅速溶解 | 无气泡产生 |
(4)Zn、NiSO4、Cu.
点评 通过金属与酸能否反应或者反应剧烈程度,金属与盐的反应,考查了金属的活动性顺序;在实验设计中要注意思维的深度和实验的严谨性.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
9.如图是物质间发生化学反应的颜色变化,其中X是( )
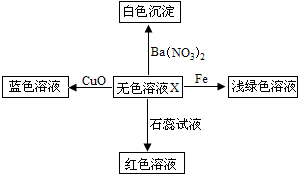

| A. | 稀硫酸 | B. | 稀盐酸 | C. | 硫酸钠溶液 | D. | 澄清石灰水 |
6.“滴水生火”魔术:向包有淡黄色过氧化钠(Na2O2)粉末的脱脂棉上滴加水,脱脂棉随即燃烧.设计实验对该“魔术”进行探究.
【提出问题】过氧化钠与水反应生成什么物质?脱脂棉为什么会燃烧?
【提出猜想】根据质量守恒定律定律,可推测出生成的气体产物可能是:氢气或氧气.
【实验1】取一支干燥的大试管,加入少量过氧化钠粉末,滴加蒸馏水,观察到试管内发生剧烈反应,产生大量气泡,用手触摸,试管底部发烫.
【实验2】为探究气体产物,进一步设计并完成如表实验.
请完成表中空格:
【查阅资料】脱脂棉是经过化学处理去掉脂肪的棉花,极易燃烧:过氧化钠能与二氧化碳反应生成碳酸钠和氧气
【实验结论】
①脱脂棉燃烧的原因过氧化钠与水反应放出热量温度达到脱脂棉的着火点,又有氧气生成,满足了燃烧的条件.
②扑灭由过氧化钠引发的火灾时,可以选择的灭火材料是C.
A.二氧化碳 B.水 C.沙子.
【提出问题】过氧化钠与水反应生成什么物质?脱脂棉为什么会燃烧?
【提出猜想】根据质量守恒定律定律,可推测出生成的气体产物可能是:氢气或氧气.
【实验1】取一支干燥的大试管,加入少量过氧化钠粉末,滴加蒸馏水,观察到试管内发生剧烈反应,产生大量气泡,用手触摸,试管底部发烫.
【实验2】为探究气体产物,进一步设计并完成如表实验.
请完成表中空格:
| 操作 | 现象 | 结论 |
| 将带火星的木条伸入试管 | 木条复燃 | 气体产物是氧气 |
【实验结论】
①脱脂棉燃烧的原因过氧化钠与水反应放出热量温度达到脱脂棉的着火点,又有氧气生成,满足了燃烧的条件.
②扑灭由过氧化钠引发的火灾时,可以选择的灭火材料是C.
A.二氧化碳 B.水 C.沙子.
3.某兴趣小组利用浓盐酸设计实验探究分子的运动,如图1所示:
(1)填写实验报告:
(2)交流讨论:
①该兴趣小组为使实验结论准确可靠,设计实验装置如图乙进行对比实验,你认为有无必要?说明理由.无必要;蒸馏水不能使酚酞变红,在第一个实验中已经可以证明了.
②将一定质量的浓盐酸盛于烧杯中,敞口放置再实验室安全之处.浓盐酸的质量和放置天数关系的曲线(见图2)正确的是乙(填写“甲”或“乙”),你选择的理由是浓盐酸具有挥发性,能挥发出溶质氯化氢,使溶液质量变小.
③若上述浓盐酸中溶剂所含氢原子数是溶质所含氢原子数的7倍,则该浓盐酸中溶质的质量分数为多少?(写出计算古过程,精确到0.1%)

(1)填写实验报告:
| 实验步骤 | 实验现象 | 分析与结论 |
| ①在盛有少量蒸馏水的烧杯中滴入2~3滴石蕊试液 | 液体显紫色 | 结论: 蒸馏水不能使酚酞变红 |
| ②在步骤①的烧杯中再滴加浓盐酸 | 试液变红 | 结论: 酸性溶液能使紫色石蕊试液变红 |
| ③按图甲所示进行实验 | 烧杯B中试液变红 | 原因: 由于浓盐酸具有较强的挥发性,所以倒扣的烧杯中会有大量的氯化氢分子存在,这些氯化氢的分子溶于烧杯B中会使该溶液变为稀盐酸而呈酸性,所以烧杯B中的紫色石蕊会变为红色,结论: 分子是不断运动的 |
①该兴趣小组为使实验结论准确可靠,设计实验装置如图乙进行对比实验,你认为有无必要?说明理由.无必要;蒸馏水不能使酚酞变红,在第一个实验中已经可以证明了.
②将一定质量的浓盐酸盛于烧杯中,敞口放置再实验室安全之处.浓盐酸的质量和放置天数关系的曲线(见图2)正确的是乙(填写“甲”或“乙”),你选择的理由是浓盐酸具有挥发性,能挥发出溶质氯化氢,使溶液质量变小.
③若上述浓盐酸中溶剂所含氢原子数是溶质所含氢原子数的7倍,则该浓盐酸中溶质的质量分数为多少?(写出计算古过程,精确到0.1%)

10.在一密闭容器内有A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得反应前后各物质的质量如下表,则下列说法中正确的是( )
| 物质 | A | B | C | D |
| 反应前物质质量(g) | 10 | 90 | 8 | 2 |
| 反应后物质质量(g) | 38 | 56 | 14 | X |
| A. | 反应中A和C的质量比为19:7 | B. | B一定是化合物 | ||
| C. | D一定是该反应的催化剂 | D. | 根据质量守恒定律,X的值为0 |
7.下列关于碳的氧化物的说法中,正确的是( )
| A. | CO2比CO多一个氧原子 | |
| B. | CO可用于冶炼铁,因为CO具有还原性 | |
| C. | CO2与CO都是大气污染物 | |
| D. | CO2能使湿润的蓝色石蕊试液变红,故CO2具有酸性 |
5.氯原子的结构示意图是( )
| A. | 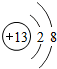 | B. | 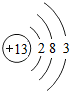 | C. | 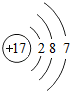 | D. | 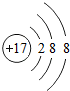 |