题目内容
10.在一密闭容器内有A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得反应前后各物质的质量如下表,则下列说法中正确的是( )| 物质 | A | B | C | D |
| 反应前物质质量(g) | 10 | 90 | 8 | 2 |
| 反应后物质质量(g) | 38 | 56 | 14 | X |
| A. | 反应中A和C的质量比为19:7 | B. | B一定是化合物 | ||
| C. | D一定是该反应的催化剂 | D. | 根据质量守恒定律,X的值为0 |
分析 本题可分析甲、乙、丙三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定丁是反应物还是生成物,进而可以确定反应类型.
解答 解:由表中数据分析可知,反应前后A的质量增加了38g-10g=28g,故A是生成物,生成的A的质量为28g;同理可以确定B是反应物,参加反应的B的质量为90g-56g=34g;C是生成物,生成的C的质量为14g-8g=6g;由质量守恒定律,D应是生成物,且生成的D的质量为34g-28g-6g=0g,故X的数值为2g+0g=2g.
A、该反应中反应中A和C的质量比为28g:6g=14:3,故选项说法错误.
B、该反应的反应物为B,生成物是A,C,D,符合“一变多”的特征,属于分解反应,故B一定是化合物,故选项说法正确.
C、D在该反应中质量不变可能是催化剂,故选项说法错误.
D、由上述分析,X的数值为=2g,故选项说法错误.
故选:B.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.

练习册系列答案
相关题目
4.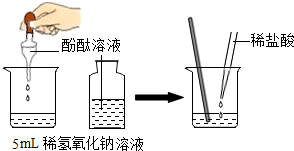 根据如图,判断以下说法错误的是( )
根据如图,判断以下说法错误的是( )
 根据如图,判断以下说法错误的是( )
根据如图,判断以下说法错误的是( )| A. | 取液后的滴管不能倒置 | B. | 用玻璃棒搅拌使反应充分 | ||
| C. | 用酚酞溶液判断该反应是否发生 | D. | 生成盐和水的反应都是酸碱反应 |
15.某兴趣小组对Zn(锌)、Ni(镍》、Cu(铜)的金属活动性顺序展开了探究.查阅了部分含镍化合物的溶解性如表,且得知镍能与酸反应.现做实验如下:
(1)同温下,取大小、厚度相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
(2)实验现象填写于表
回答下列问题:
(1)上述实验步骤有欠缺,请设计完善实验前,应用砂纸打磨三种金属,除去表面的氧化膜.
(2)将表格中实验现象填写完整.
(3)得出Zn,Ni(镍)、Cu的金属活动性顺序是Zn>Ni>Cu,写出镍与盐酸反应的化学方程式Ni+2HCl=NiCl2+H2↑.
(4)请选择另一类别的一种试剂设计实验.也同样达到一次验证上述假设的正确与否.写出你选择试剂的化学式Zn、NiSO4、Cu.
(1)同温下,取大小、厚度相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
| 阴离子 镍离子 | OH- | NO3- | SO42- | Cl- |
| Ni2+ | 不 | 溶 | 溶 | 溶 |
| 金属 | Ni | Zn | Cu |
| 与盐酸反应的现象 | 气体产生缓慢 金属逐渐溶解 | 气体产生激烈金属迅速溶解 | 无气泡产生 |
(1)上述实验步骤有欠缺,请设计完善实验前,应用砂纸打磨三种金属,除去表面的氧化膜.
(2)将表格中实验现象填写完整.
(3)得出Zn,Ni(镍)、Cu的金属活动性顺序是Zn>Ni>Cu,写出镍与盐酸反应的化学方程式Ni+2HCl=NiCl2+H2↑.
(4)请选择另一类别的一种试剂设计实验.也同样达到一次验证上述假设的正确与否.写出你选择试剂的化学式Zn、NiSO4、Cu.
2.“类推”是化学学习过程中常用的思维方法.现有以下类推结果,其中正确的是( )
| A. | 因为酸溶液呈酸性,所以呈酸性的溶液一定是酸溶液 | |
| B. | 生铁和钢都是铁的合金,所以其物理性能完全相同 | |
| C. | 金属铝与盐酸反应生成A1C13和H2,所以金属铁与盐酸反应生成FeC13和H2 | |
| D. | 高锰酸钾中含有氧元素,它受热分解可以产生氧气,所以能分解产生氧气的物质一定含有氧元素 |
19.下列过程属于化学变化的是( )
| A. | 石蜡熔化 | B. | 电解水 | C. | 水力发电 | D. | 干冰制冷 |
20.下列不属于塑料性能的是( )
| A. | 密度小 | B. | 易导电 | C. | 易加工 | D. | 耐腐蚀 |

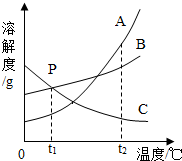 如图是A、B、C三种固体物质的溶解度曲线图.
如图是A、B、C三种固体物质的溶解度曲线图.