题目内容
20. 某个化学反应的微观示意图下如图所示.下列有关说法错误的是( )
某个化学反应的微观示意图下如图所示.下列有关说法错误的是( )| A. | 该反应为化合反应 | |
| B. | 该反应不遵守质量守恒定律 | |
| C. | 该反应前后分子总数未发生变化 | |
| D. | 该反应的化学方程式为H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl |
分析 根据反应过程图中的分子,判断反应物与生成物,结合化学变化的实质是分子分成原子,原子重新组合成新分子,进行分析判断.
解答 解:由化学反应的微观示意图可知:该反应的化学方程式为H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl;
A、该反应符合多变一,为化合反应,故选项说法正确.
B、化学反应都遵守质量守恒定律,故选项说法错误.
C、该反应前后分子总数未发生变化,都为2个,故选项说法正确.
D、该反应的化学方程式为H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl;故选项说法正确.
答案:B
点评 本题通过微观粒子的反应模型图,考查了微观上对化学反应的认识,学会通过微观示意图把宏观物质和微观粒子联系起来、从微观的角度分析物质的变化是正确解答此类题的关键.

练习册系列答案
相关题目
10.下列是某同学在填写实验报告册时描述的实验现象,其中正确的是( )
| A. | 将氢氧化钠溶液滴入硫酸铜溶液中,产生蓝色沉淀 | |
| B. | 在稀盐酸中滴入石蕊试液,石蕊试液变成蓝色 | |
| C. | 在燃着的CO火焰上罩冷而干燥的烧杯,烧杯内壁出现小水珠 | |
| D. | 硫在氧气中燃烧时,产生白烟,生成有刺激性气味的气体 |
15.下列各组溶液中,只需加酚酞试液就可鉴别开的一组是( )
| A. | HCl、NaOH、KOH | B. | NaCl、NaOH、KNO3 | C. | NaCl、NaOH、H2SO4 | D. | HCl、NaOH、H2SO4 |
9.类推是学习中常用的思维方法,现有以下类推结果,其中错误的是( )
①碱的水溶液通常呈碱性,所以碱性溶液一定是碱的溶液②氧化物都含有氧元素,所以含氧元素的化合物一定是氧化物③碱中一定含有金属离子.酸碱发生中和反应生成盐和水,所以生成水的反应一定是中和反应.
①碱的水溶液通常呈碱性,所以碱性溶液一定是碱的溶液②氧化物都含有氧元素,所以含氧元素的化合物一定是氧化物③碱中一定含有金属离子.酸碱发生中和反应生成盐和水,所以生成水的反应一定是中和反应.
| A. | 只有① | B. | ①② | C. | ①③ | D. | ①②③ |
3.如表是Ca(OH)2和NaOH的溶解度随温度变化的数据.请回答下列问题: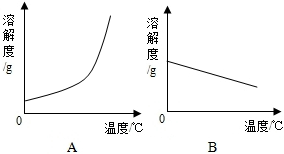
(1)依据如表数据,绘制Ca(OH)2和NaOH的溶解度曲线,如图所示能表示NaOH溶解度曲线的是A(填序号)
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,下列具体措施中正确有①②⑤⑥(填序号).
①加入氢氧化钙 ②升高温度 ③降低温度
④加入水 ⑤蒸发水后再恢复到原温度 ⑥加入生石灰
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为91g.
(4)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶并过滤.

| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
| Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,下列具体措施中正确有①②⑤⑥(填序号).
①加入氢氧化钙 ②升高温度 ③降低温度
④加入水 ⑤蒸发水后再恢复到原温度 ⑥加入生石灰
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为91g.
(4)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶并过滤.
 学习过中和反应之后,小城绘制了氢氧化钠溶液和稀盐酸反应的微观模拟图.
学习过中和反应之后,小城绘制了氢氧化钠溶液和稀盐酸反应的微观模拟图. 的结构示意图;
的结构示意图; 如图所示是医院常用的药瓶和注射器,请你据图回答:
如图所示是医院常用的药瓶和注射器,请你据图回答: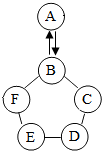 如图所示的是物质A~F相互间的关系(“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).通常情况下A是能参与绿色植物光合作用的气体;B是工业上广泛用于玻璃、造纸、纺织和洗涤剂生产等领域;D的溶液呈蓝色;E搜地壳中含量最多的金属元素的单质.请回答下列问题.
如图所示的是物质A~F相互间的关系(“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).通常情况下A是能参与绿色植物光合作用的气体;B是工业上广泛用于玻璃、造纸、纺织和洗涤剂生产等领域;D的溶液呈蓝色;E搜地壳中含量最多的金属元素的单质.请回答下列问题.