题目内容
某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后,过滤、洗涤、干燥、称重,得到的实验数据如下:| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
(2)计算合金样品中镁的质量分数______;
(3)计算所用稀硫酸中溶质的质量分数______(计算结果保留到0.1%);
(4)第六次实验后,所得溶液中硫酸镁的质量分数(要求写出计算过程,结果保留到0.1%).
【答案】分析:(1)根据表格中的数据可分析出与10克稀硫酸恰好完全反应的镁的质量,进而可确定m的值;
(2)反应前后固体物质减少的质量为镁的质量,根据质量分数的计算公式可以求出镁铜合金中镁的质量分数;
(3)根据10g硫酸只能消耗0.5g镁进行计算,算出硫酸质量,再除以10g乘以百分之百即可;
(4)根据表格中数据利用镁与硫酸反应的化学方程式,根据镁的质量反应后溶液中硫酸镁的质量,然后根据求出反应后溶液中溶质的质量分数即可.
解答:解:(1)因为铜不与硫酸反应,因此最后剩余的0.6g固体的成分是铜;从表格数据可知,每10g硫酸就消耗0.5g镁,因此mg=3g-0.5g=2.5g,
(2)结合(1)的解答并分析题中数据可以知道第六次和第五次加入稀盐酸后金属的质量没有改变,所以可以判断铜的质量为0.6g,所以镁的质量分数为=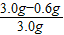 ×100%=80%.
×100%=80%.
(3)设10克稀硫酸中所含H2SO4的质量为x.
Mg+H2SO4=MgSO4+H2↑
24 98
0.5g x 根据: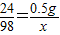 解得:x=2.04g
解得:x=2.04g
稀硫酸的溶质质量分数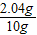 ×100%=20.4%.
×100%=20.4%.
(4)设生成硫酸镁的质量为y,氢气质量为z
Mg+H2SO4═MgSO4+H2↑
24 120 2
2.4g y z
根据: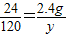 解得:y=12g 根据:
解得:y=12g 根据: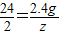 解得z=0.2g
解得z=0.2g
第五次加入稀硫酸后所得溶液中硫酸镁的质量分数为: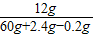 x100%=19.3%
x100%=19.3%
答:第五次加入稀硫酸后所得溶液中硫酸镁的质量分数为19.3%
故答案为:(1)2.5g;(2)80%;(3)20.4%;(4)19.3%.
点评:本考点考查了表格型计算题,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,还要记牢“遇到差值要想气体”.本考点主要出现在计算题中.
(2)反应前后固体物质减少的质量为镁的质量,根据质量分数的计算公式可以求出镁铜合金中镁的质量分数;
(3)根据10g硫酸只能消耗0.5g镁进行计算,算出硫酸质量,再除以10g乘以百分之百即可;
(4)根据表格中数据利用镁与硫酸反应的化学方程式,根据镁的质量反应后溶液中硫酸镁的质量,然后根据求出反应后溶液中溶质的质量分数即可.
解答:解:(1)因为铜不与硫酸反应,因此最后剩余的0.6g固体的成分是铜;从表格数据可知,每10g硫酸就消耗0.5g镁,因此mg=3g-0.5g=2.5g,
(2)结合(1)的解答并分析题中数据可以知道第六次和第五次加入稀盐酸后金属的质量没有改变,所以可以判断铜的质量为0.6g,所以镁的质量分数为=
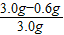 ×100%=80%.
×100%=80%.(3)设10克稀硫酸中所含H2SO4的质量为x.
Mg+H2SO4=MgSO4+H2↑
24 98
0.5g x 根据:
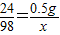 解得:x=2.04g
解得:x=2.04g稀硫酸的溶质质量分数
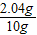 ×100%=20.4%.
×100%=20.4%.(4)设生成硫酸镁的质量为y,氢气质量为z
Mg+H2SO4═MgSO4+H2↑
24 120 2
2.4g y z
根据:
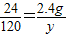 解得:y=12g 根据:
解得:y=12g 根据: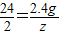 解得z=0.2g
解得z=0.2g第五次加入稀硫酸后所得溶液中硫酸镁的质量分数为:
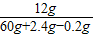 x100%=19.3%
x100%=19.3%答:第五次加入稀硫酸后所得溶液中硫酸镁的质量分数为19.3%
故答案为:(1)2.5g;(2)80%;(3)20.4%;(4)19.3%.
点评:本考点考查了表格型计算题,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,还要记牢“遇到差值要想气体”.本考点主要出现在计算题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某化学兴趣小组为了分析生铁中铁的含量,进行了实验研究,即取60g经粉碎后的生铁,把800稀硫酸分4次加入到该样品中,测得数据记录如下表:

(说明:生铁中杂质不溶于水,也不与硫酸反应.)
(1)第2次测得剩余固体质量为15.2g,其成分为 .
A.铁 B.铁和碳 C.碳
(2)生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)
(3)计算所用稀硫酸的溶质质量分数为多少?(写出计算过程,结果保留到小数点后一位)并画出反应生成的氢气质量与加入稀硫酸质量的关系图.
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀硫酸质量(g) | 200 | 200 | 200 | 200 |
| 剩余固体质量(g) | 37.6 | 15.2 | 4 | 4 |

(说明:生铁中杂质不溶于水,也不与硫酸反应.)
(1)第2次测得剩余固体质量为15.2g,其成分为
A.铁 B.铁和碳 C.碳
(2)生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)
(3)计算所用稀硫酸的溶质质量分数为多少?(写出计算过程,结果保留到小数点后一位)并画出反应生成的氢气质量与加入稀硫酸质量的关系图.
我市某地盛产石灰石,其中含有不溶于盐酸的杂质.某化学兴趣小组为了测定石灰石中碳酸钙的含量,取10.0g石灰石样品,经粉碎后全部放入烧杯中,并加入足量的稀盐酸,烧杯及所盛物质的总质量为80.0g.反应过程中测得烧杯及所盛物质的质量与相应时间记录如下表:
试计算:(1)反应结束后,共放出多少克的二氧化碳?
(2)该石灰石样品中碳酸钙的质量分数是多少?
| 反应时间/分 | 0 | 2 | 4 | 6 | 8 | 10 |
| 烧杯及所盛物质质量/克 | 80.0 | 79.0 | 78.3 | 77.9 | 77.8 | 77.8 |
(2)该石灰石样品中碳酸钙的质量分数是多少?
 某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验.实验装置如图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止.测得反应前后的有关质量如表:
某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验.实验装置如图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止.测得反应前后的有关质量如表:
