题目内容
氢化钙(CaH2)是一种重要的制氢剂,与水接触时,发生反应生成氢氧化钙和氢气。
1.写出该反应的化学方程式。
2.若需要40 g氢气,计算至少需要消耗氢化钙的质量。
【答案】
1.CaH2 + 2H2O=Ca(OH)2 + 2H2↑
2.420g
【解析】可根据氢气的质量,利用化学方程式,列出比例式,求出氢化钙的质量,进行解答
【解】设:至少需要消耗氢化钙的质量为x。
CaH2 + 2H2O=Ca(OH)2 + 2H2↑
42 4
x 40 g
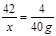
x = 420 g

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目