题目内容
8.某兴趣小组同学对6g氯酸钾和二氧化锰的混合物进行研究.依次加热该混合物t1、t2、t3、t4时间,再冷却后称量剩余物质质量,记录有关数据如下表(样品中的杂志不参加反应):| 加热时间/min | t1 | t2 | t3 | t4 |
| 剩余固体的质量/g | 4.24 | 4.16 | 4.08 | 4.08 |
(2)加热过程中,剩余固体质量变小的原因是氯酸钾分解生成的氧气逸出;加热至t3时间后,剩余固体的质量不在改变,其原因是加热至t3时间后,氯酸钾已经完全分解.
分析 (1)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,写出反应的化学方程式即可.
(2)根据质量守恒定律,氯酸钾分解生成的氧气逸出,结合氯酸钾已经完全分解后,剩余固体质量不再改变,进行分析解答.
解答 解:(1)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(2)加热过程中,剩余固体质量变小的原因是氯酸钾分解生成的氧气逸出;加热至t3时间后,剩余固体的质量不在改变,是因为时间为t3时氯酸钾已经完全分解.
答:(1)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;(2)氯酸钾分解生成的氧气逸出;加热至t3时间后,氯酸钾已经完全分解.
点评 本题难度不大,实验室加热氯酸钾制取氧气的反应原理并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
19.为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如下所示:

下列说法正确的是( )

下列说法正确的是( )
| A. | 该反应中涉及两种氧化物 | |
| B. | 该反应类型为化合反应 | |
| C. | 该反应中反应物两种分子的个数比为3:1 | |
| D. | 反应前后物质的种类保持不变 |
3.下列有关熟石灰的说法错误的是( )
| A. | 熟石灰又称为消石灰 | |
| B. | 熟石灰由生石灰与水反应而制得 | |
| C. | 熟石灰的水溶液在空气中久置后溶液质量会增加 | |
| D. | 石灰水即熟石灰的水溶液,能使紫色石蕊试液变蓝 |
19.下列物质与水混合,在室温时难以形成饱和溶液的是( )
| A. | CO2 | B. | CuSO4 | C. | C2H5OH | D. | KNO3 |
 以图(1)和图(2)是两个设计证明分子运动的实验.在图(2)的锥形瓶中的小瓶里装着浓氨水,锥形瓶口用一张滤纸盖住,滤纸刚刚用酚酞溶液浸过.
以图(1)和图(2)是两个设计证明分子运动的实验.在图(2)的锥形瓶中的小瓶里装着浓氨水,锥形瓶口用一张滤纸盖住,滤纸刚刚用酚酞溶液浸过.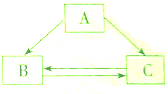 碳及其氧化物之间存在如图所示的相互转化关系,其中B是A不充分燃烧的产物.请回答下列问题:
碳及其氧化物之间存在如图所示的相互转化关系,其中B是A不充分燃烧的产物.请回答下列问题: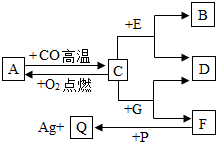 现有A、B、C、D、E、F、G、P、Q九种物质,其中A为磁铁矿的主要成分,C、F是常见金属,B是相对分子质量最小的气体单质,D为浅绿色溶液,G为蓝色溶液.它们之间关系如图所示,试推测:
现有A、B、C、D、E、F、G、P、Q九种物质,其中A为磁铁矿的主要成分,C、F是常见金属,B是相对分子质量最小的气体单质,D为浅绿色溶液,G为蓝色溶液.它们之间关系如图所示,试推测:
