题目内容
5.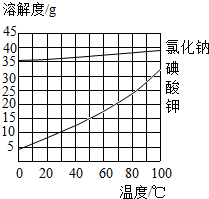 “食盐加碘”通常是在氯化钠中加入碘酸钾.如图所示是氯化钠和碘酸钾的溶解度曲线图.下列说法正确的是( )
“食盐加碘”通常是在氯化钠中加入碘酸钾.如图所示是氯化钠和碘酸钾的溶解度曲线图.下列说法正确的是( )| A. | 氯化钠和碘酸钾均为易溶于水的物质 | |
| B. | 氯化钠和碘酸钾的溶解度随温度升高而增大 | |
| C. | 20℃时,不可能制得质量分数为20%氯化钠溶液 | |
| D. | 升高温度,碘酸钾的溶解速率加快,而氯化钠的溶解速率不变 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、在20℃时,碘酸钾的溶解度小于10g,所以碘酸钾属于可溶物质,故A错误;
B、通过分析溶解度曲线可知,氯化钠和碘酸钾的溶解度随温度升高而增大,故B正确;
C、20℃时,不会氯化钠溶液的质量分数为:$\frac{36g}{100g+36g}$×100%=26.5%,所以不可能制得质量分数为20%氯化钠溶液,故C错误;
D、升高温度,碘酸钾的溶解速率加快,而氯化钠的溶解速率变化不大,故D错误.
故选:B.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
16.某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验:

(1)A试管中滴加稀盐酸后,可观察到的现象是产生气泡,溶液由无色变为浅绿色,发生反应的化学方程式为Fe+2HCl═FeCl2+H2↑;
(2)写出B试管中反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究:
【提出猜想】
甲同学猜想:NaCl;
乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、HCl;
丁同学猜想:NaCl、Na2CO3.
【查阅资料】NaCl、CaCl2溶液均呈中性.
【交流讨论】甲同学认为丙同学的猜想一定不正确,理由是:白色沉淀是CaCO3,CaCO3能和稀盐酸反应,二者不能共存.
【设计实验】乙、丁两位同学分别设计如下实验验证自己的猜想:
【反思评价】实验结束后,甲同学认为乙(填“乙”或“丁”)同学的实验结论错误,原因是若溶质只有氯化钠,滴加无色酚酞试液时,酚酞试液也不变色.

(1)A试管中滴加稀盐酸后,可观察到的现象是产生气泡,溶液由无色变为浅绿色,发生反应的化学方程式为Fe+2HCl═FeCl2+H2↑;
(2)写出B试管中反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究:
【提出猜想】
甲同学猜想:NaCl;
乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、HCl;
丁同学猜想:NaCl、Na2CO3.
【查阅资料】NaCl、CaCl2溶液均呈中性.
【交流讨论】甲同学认为丙同学的猜想一定不正确,理由是:白色沉淀是CaCO3,CaCO3能和稀盐酸反应,二者不能共存.
【设计实验】乙、丁两位同学分别设计如下实验验证自己的猜想:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 乙 | 取少量滤液于试管中,向其中滴加无色酚酞试液 | 无明显现象 | 猜想正确 |
| 丁 | 取少量滤液于试管中,向其中滴加稀盐酸 | 有气泡产生 | 猜想正确 |
20.“归纳与比较”是化学学习的重要方法.下列对氧气和二氧化碳的异同点比较错误的是( )
| A. | 组成:氧气只由氧元素组成,二氧化碳由碳氧两种元素组成 | |
| B. | 性质:氧气能使带火星的木条复燃,二氧化碳能使燃着的木条熄灭 | |
| C. | 制备:实验室中制取氧气和二氧化碳的发生装置和收集装置一定相同 | |
| D. | 用途:氧气主要用于供给呼吸、支持燃烧等,二氧化碳用于人工降雨、灭火等 |
17.骑自行车是人们喜爱的一种运动.许多市民骑自行车上下班.从环保角度看,这主要是有利于减少城市的( )
| A. | 大气污染 | B. | 水污染 | C. | 土壤污染 | D. | 白色污染 |
15.下列实验方案设计可行的是( )
| A. | 用溶解、过滤的方法分离氯化钠和硝酸钾的固体混合物 | |
| B. | 用酚酞鉴别氢氧化钠溶液和碳酸钠溶液 | |
| C. | 向氧化铜中加入适量稀硫酸恰好反应后,再加入适量氢氧化钡溶液,过滤即可制得氢氧化铜 | |
| D. | 向某无色溶液中加入足量稀盐酸无现象,再加入氯化钡溶液,若产生白色沉淀,证明原溶液中一定含有SO42- |


 已知A、B、C、D、E、F、G均为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,它们之间的相互转化关系如图所示:
已知A、B、C、D、E、F、G均为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,它们之间的相互转化关系如图所示: 如图是初中化学实验的几种常用仪器,请按要求填空.
如图是初中化学实验的几种常用仪器,请按要求填空.