题目内容
15.A-G是初中常见的物质.其中E为黑色固体.如图为这些物质的转化关系图,其中部分生成物和反应条件已省略.
(1)写出下列物质的化学式:ECuO,GCuSO4.
(2)化学反应常伴有能量变化.B与水反应时会放出(“吸收”或“放出”)热量.
(3)实验室不用A与稀硫酸反应来制取C,原因是反应生成的CaSO4微溶于水,包在CaCO3表面,阻止反应继续进行.
(4)写出D→F的化学方程式Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(5)可用Cu、O2和H2SO4作原料制得CuSO4,反应的化学方程式是2Cu+O2 $\frac{\underline{\;\;△\;\;}}{\;}$2CuO;CuO+H2SO4═CuSO4+H2O.
分析 根据题干叙述,A高温能生成B和C,故A可能碳酸钙,生成的B和C是氧化钙和二氧化碳,B能与水反应生成的,故B可能是氧化钙,D是氢氧化钙,氢氧化钙能与碳酸钠反应生成F,F能与G反应生成蓝色沉淀,故F是氢氧化钠,F是硫酸铜,E能与硫酸反应生成硫酸铜,故E是氧化铜,氧化铜能与一氧化碳反应生成铜和二氧化碳,据此解答.
解答 解:A高温能生成B和C,故A可能碳酸钙,生成的B和C是氧化钙和二氧化碳,B能与水反应生成的,故B可能是氧化钙,D是氢氧化钙,氢氧化钙能与碳酸钠反应生成F,F能与G反应生成蓝色沉淀,故F是氢氧化钠,F是硫酸铜,E能与硫酸反应生成硫酸铜,故E是氧化铜,氧化铜能与一氧化碳反应生成铜和二氧化碳,带入框图,推断合理;
(1)E是氧化铜,G是硫酸铜,故填:CuO,CuSO4;
(2)氧化钙与水反应会放出热量,故填:放出;
(3)碳酸钙与硫酸反应生成的CaSO4微溶于水,包在CaCO3表面,阻止反应继续进行,故填:反应生成的CaSO4微溶于水,包在CaCO3表面,阻止反应继续进行;
(4)氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故填:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(5)用Cu、O2和H2SO4作原料制得CuSO4,首先铜与氧气在加热条件下生成氧化铜,反应化学方程式为2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;氧化铜再与硫酸反应生成硫酸铜和水,反应的化学方程式为CuO+H2SO4═CuSO4+H2O;
答案:2Cu+O2 $\frac{\underline{\;\;△\;\;}}{\;}$2CuO;CuO+H2SO4═CuSO4+H2O.
点评 本题为框图式物质推断题,解答本题的关键是找准解题的突破口,直接得出有关物质的化学式,然后根据框图结合物质的性质推断得出其他物质的化学式.

 某同学分别将浸过食盐水的铁丝绒,浸过蒸馏水的铁丝绒和干燥的铁丝绒放入大小相同的试管A、B、C中,进行如图所示的实验,测插在烧杯里的玻璃管中水上升的高度.实验结果记录如下表
某同学分别将浸过食盐水的铁丝绒,浸过蒸馏水的铁丝绒和干燥的铁丝绒放入大小相同的试管A、B、C中,进行如图所示的实验,测插在烧杯里的玻璃管中水上升的高度.实验结果记录如下表| 时间/h | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A上升高度/cm | 0 | 0.4 | 3.3 | 5.6 | 6.8 | 9.8 | 13.5 |
| B上升高度/cm | 0 | 0 | 0 | 0 | 0 | 0.5 | 1.0 |
| C上升高度/cm | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| A. | 实验中可能影响铁生锈的因素之一为铁丝绒浸泡过的液体的种类 | |
| B. | 如果使用较细的玻璃管,则A中试管内液面上升的高度会增加 | |
| C. | 该试验说明铁生锈与空气和水有关. | |
| D. | 继续放置一段时间后,最终C中玻璃管内液面也会上升 |
| A. | 可能存在Cl- | B. | 一定存在CO32-,一定不存在Ba2+ | ||
| C. | 一定存在Na+ | D. | 一定存在SO42-,可能存在Ca2+ |
【提出问题】硫酸铜溶液是不是此反应的催化剂?硫酸铜溶液的体积对此实验有影响吗?
【设计并实验】室温下,小明将过量、表面积相同已打磨的铝片分别加入到6份30mL10%稀盐酸中,并在每份中加入不同体积的硫酸铜饱和溶液,记录获得相同体积氢气的时间,从而确定产生氢气的速率.
| 实验混合溶液 | 1 | 2 | 3 | 4 | 5 | 6 |
| 饱和硫酸铜溶液/mL | 0 | 0.5 | 2.5 | 5 | 10 | 20 |
| 水/mL | 20 | 19.5 | 17.5 | V | 10 | 0 |
(2)写出铝和稀盐酸反应的化学方程式2Al+6HCl═2AlCl3+3H2↑:
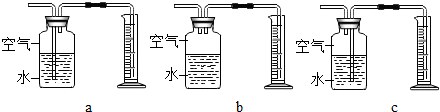
(3)定量收集氢气体积可用如图c(填写字母序号)装置.
【实验现象】随着硫酸铜溶液体积的增加,产生氢气的速率先加快后明显减慢,且铝片表面附着的红色物质逐渐增加.
【结论与解释】
(4)随着硫酸铜体积的增加,反应速率明显变慢可能的原因是部分铝和硫酸铜溶液发生了置换反应;
(5)根据实验现象小明认为硫酸铜溶液不是此反应的催化剂,其原因是硫酸铜质量发生了改变且和铝发生了反应;
【实验反思】加速铝和稀硫酸反应速率还可以采取的措施是(写出一点)提高温度,增大盐酸浓度等.
【实验拓展】根据上述实验,小明认为是盐中的金属离子影响了铝和稀盐酸的反应速率;为了研究不同金属离子对反应的影响,小明同学继续实验,取过量表面积相同的铝片和30mL10%稀盐酸混合后加入不同的盐溶液,实验现象如表(加号越多,代表反应速率越快):
| 实验1 | 实验2 | 实验3 | 实验4 | 实验5 | |
| 加入试剂0.5mL | 水 | 5%NaCl溶液 | 5%Mg(NO3)2溶液 | 5%FeSO4溶液 | 5%CuSO4溶液 |
| 产生气泡速率 | + | + | + | ++ | +++ |
(7)上述实验设计存有缺陷,该缺陷是铝片未经过表面打磨;实验改进后,任符合上表中的实验现象,可得到的实验结论是:
①Na+、Mg2+ 对实验效果没有明显效果;②Fe2+、Cu2+能加快铝和稀盐酸反应的速率,且Cu2+ 效果最好.
| A. | 冷却硝酸钾的热饱和溶液有硝酸钾晶体析出 | |
| B. | 水蒸气液化成水 | |
| C. | 水通电可以得到氢气和氧气 | |
| D. | 蔗糖放入水中不见了 |
| A. | 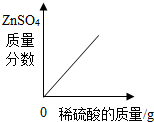 向一定量锌粒中加入过量稀硫酸 向一定量锌粒中加入过量稀硫酸 | |
| B. |  向一定量氯化钠饱和溶液中不断加入水 向一定量氯化钠饱和溶液中不断加入水 | |
| C. | 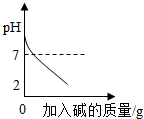 向pH=2的溶液中加入碱性溶液 向pH=2的溶液中加入碱性溶液 | |
| D. |  向一定量氢氧化钠和碳酸钠的混合溶液中加入稀盐酸 向一定量氢氧化钠和碳酸钠的混合溶液中加入稀盐酸 |
 实验室有一瓶敞口存放的氢氧化钠,小明在做实验时发现已部分变质.他称取变质的氢氧化钠样品15克放入烧杯,加适量蒸馏水配制成溶液,再向其中滴加CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl).反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:
实验室有一瓶敞口存放的氢氧化钠,小明在做实验时发现已部分变质.他称取变质的氢氧化钠样品15克放入烧杯,加适量蒸馏水配制成溶液,再向其中滴加CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl).反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题: